Malformații cardiace congenitale. Malformații cardiace congenitale la adulți
Malformațiile cardiace congenitale sunt un grup de boli cu șunturi intracardiace, anomalii în localizarea structurilor inimii, modificări valvulare și multe alte malformații care apar în perioada embrionară. Un grup destul de mare de astfel de pacienți supraviețuiește până la vârsta adultă. De regulă, pacienții au semne distincte și mai presus de toate auscultatorii de defect, modificări ECG, radiografii ale inimii. Ecocardiografia are o importanță decisivă în diagnosticul inițial. Cateterismul cardiac și angiografia confirmă diagnosticul. Unii dintre pacienți sunt indicați pentru tratament chirurgical, alții trebuie observați pentru a fi îndrumați la un moment dat la un chirurg cardiac și încă alții interventie chirurgicala nu se mai arată, dar au nevoie de terapie conservatoare.
Cuvinte cheie: defecte cardiace congenitale.
introducere
Defect cardiac congenital(CHD) este o boală care apare în perioada dezvoltării embrionare. Printre destule un numar mare cunoscute malformații congenitale și anomalii ale inimii, există cele cu care pacientul trăiește până la vârsta adultă. Acest lucru se explică prin faptul că o serie de boli din acest grup se manifestă puțin în copilărie, sunt asimptomatice pentru o lungă perioadă de timp sau cu simptome șterse. În același timp, eficacitatea tratamentului medicamentos modern al insuficienței cardiace și decompensarea acesteia este atât de mare încât, în unele cazuri, viața pacientului este prelungită, iar etiologia bolii rămâne neclară. Și deși acești pacienți trăiesc până la vârsta adultă, ei mor în mai mult Varsta frageda decât în populaţia cu insuficienţă cardiacă
sau brusc, în timp ce corecția chirurgicală la unele dintre ele ar putea prelungi viața. Din diverse motive, mulți dintre pacienții mai în vârstă grupă de vârstă nu sunt supuse tratamentului chirurgical. Pentru un grup de pacienți inoperabili, se dezvoltă metode de tratament conservator (medicament) care le pot îmbunătăți starea și chiar le pot prelungi viața (T. Adriaenssens et al, 2006, G.-P. Diller, 2006). Unii dintre ei li se arată un transplant de inimă și plămâni. Prin urmare, diagnosticul de CHD la un pacient adult este o sarcină urgentă.
clasificarea malformațiilor cardiace congenitale
Exista diverse clasificări CHD, care se bazează în principal pe descrierea anatomiei leziunilor cardiace (clasificarea defectelor cardiace și vasculare congenitale, OMS, 1976). În opinia noastră, clasificarea care reflectă prevalența defectului și capacitatea unui pacient care suferă de acesta de a trăi fără tratament chirurgical timp de 15-17 ani sau mai mult contribuie la cel mai mult abordare corectă la diagnosticul acestor boli la adulți (N. Schiller, M.A. Osipov, 2005). În conformitate cu această clasificare, toate HPU-urile sunt împărțite în patru grupuri:
1) comune, în prezența cărora pacienții supraviețuiesc adesea până la vârsta adultă;
2) rare, în prezența cărora pacienții supraviețuiesc până la vârsta adultă;
3) frecvente, în prezența cărora pacienții supraviețuiesc rar până la vârsta adultă;
4) rare, în prezența cărora pacienții de cele mai multe ori nu trăiesc până la vârsta adultă.
diagnostice
Evaluarea tabloului clinic
1. În fruntea tabloului clinic cu CHD se află un suflu aspru, cel mai adesea sistolic, în zona inimii, care
auzit din copilărie. Localizarea acestui zgomot este cel mai adesea la stânga sternului în al 2-lea, al 3-lea, al 4-lea spațiu intercostal. Unii pacienți nu au zgomot, dar vorbesc despre zgomotul pe care l-au auzit în copilărie și apoi a dispărut. O astfel de situație apare, de exemplu, atunci când presiunea din ventriculi se egalizează cu un defect septal atrial, descărcarea se oprește și zgomotul dispare pentru un timp.
2. Fizicul zvelt al pacienților (scădere în greutate) sau statură mică. Fizicul unui adult în astfel de cazuri seamănă cu fizicul unui copil. Unii dintre acești pacienți au grade diferite de cianoză. În unele cazuri, pacienții merg la medic când dezvoltă insuficiență cardiacă cu edem și un ficat mărit.
3. Informații despre prematuritate sau întârzierea dezvoltării în copilărie, cianoză, oboseală în timpul efortului sau în timpul hrănirii. Aceștia sunt așa-numiții răpiți slabi pruncie sau copii care nu suportă activitate fizica la egalitate cu ceilalți copii. Există și prezența durerii în inimă din primii ani de viață, pneumonie frecventă.
4. Anomalii extracardiace congenitale mari, cum ar fi buza despicată, palatul dur, ptoza, deformarea cufăr, polidactilie, despicarea oaselor mâinii etc. Uneori se dezvăluie patologia organelor interne, de exemplu, diverticuloza tractului gastrointestinal, hipoplazia pulmonară etc.
5. Micile anomalii extracardiace congenitale (mici stigmate) sunt dismorfisme faciale, cum ar fi microftalmia sau flatul pliul pieliiîntre nas și buza superioară, hipoplazia maxilarului, prezența epicantului, displasticitatea generală a corpului.
6. Informații despre bolile care au apărut la mama pacientului în timpul dezvoltarea prenatală copil, cum ar fi rubeola la mamă în timpul sarcinii.
Astfel, există un set de date clinice care pot sugera CHD la un pacient adult.
Electrocardiografie
Simptomele clinice, identificate în primul rând, adesea în perioada asimptomatică, murmurul în zona inimii sunt cele care ne fac să ne gândim la un defect congenital. Electrocardiografia în 12 derivații clasice - cea mai simplă și cea mai des folosită
Metoda de diagnosticare a bolilor cardiace este de mare ajutor în stadiul inițial al diagnosticării malformațiilor cardiace congenitale. Modificările ECG nu sunt specifice unuia sau altui defect, ele sunt adesea detectate întâmplător și sunt cel mai adesea reprezentate de semne de hipertrofie severă a oricărei părți a inimii, mai des ventriculul drept, dar uneori cel stâng sau ambele, suprasolicitarea atrială. Poate fi, de asemenea, bloc AV inexplicabil sau alte tulburări de ritm sau de conducere care au fost identificate încă din copilărie. Adesea, semnele de boală cardiacă congenitală sunt detectate pentru prima dată când se efectuează un ECG.
examinare cu raze X
În ciuda introducerii pe scară largă diverse tehnici imagistica inimii, radiografia toracica ramane o metoda destul de informativa. Cu ajutorul acestuia, se evaluează configurația inimii, valoarea fluxului sanguin pulmonar, severitatea pulsației rădăcinilor plămânilor, se detectează o creștere a camerelor inimii.
ecocardiografie
Ecocardiografia bidimensională este o metodă care permite vizualizarea structurilor inimii și este ideală pentru diagnosticarea bolilor cardiace congenitale. Capacitatea de a vizualiza dintr-o varietate de accese vă permite să evaluați anatomia și relația dintre camerele inimii, iar ecocardiografia Doppler vă permite să identificați șunturile intracardiace și extracardiace. În același timp, diagnosticul bolilor cardiace congenitale folosind ecocardiografia transtoracică la un copil, datorită dimensiunilor sale mici și absenței modificărilor osoase și pulmonare legate de vârstă, este mult mai ușor decât la adulți.
În timpul examinării inițiale folosind o ecocardiografie bidimensională, o examinare secvențială și sistematică a inimii trebuie efectuată din mai multe abordări: de la abord parasternal cu examinare de-a lungul axei lungi și la diferite niveluri ale axei scurte, de la abordul apical. cu examinare în poziții cu patru și două camere, din abordul subcostal și suprasternal cu un studiu al inimii de-a lungul axelor lungi și scurte (vezi capitolul „Ecocardiografie”). Acest lucru va face posibilă evaluarea poziției relative a camerelor inimii, pentru a identifica o rupere a structurilor sale.
Din cauza dificultăților care apar la examinarea pacienților adulți cu ajutorul ecocardiografiei transtoracice, ecocardiografia transesofagiană devine o metodă de verificare. Cu acces transesofagian, senzorul de înaltă frecvență este situat aproape de obiect și „vede” foarte bine piese mici. Pe fig. Figurile 11.1 A și B prezintă ecocardiografia transesofagiană și Doppler color la un pacient adult cu un defect primar de IVS.
Orez. 11.1 A. Ecocardiografia transesofagiană a unui pacient cu VSD primară
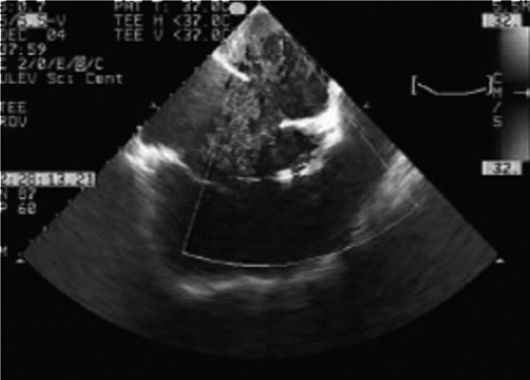 Orez. 11.1 B. Ecocardiografie transesofagiană și Doppler color (vezi insert) la același pacient. Fluxul sanguin turbulent prin defect este clar vizibil
Orez. 11.1 B. Ecocardiografie transesofagiană și Doppler color (vezi insert) la același pacient. Fluxul sanguin turbulent prin defect este clar vizibil
Metode de clarificare
Astfel de metode includ în prezent imagistica prin rezonanță magnetică a inimii și tomografia computerizată multislice. Ambele metode sunt foarte precise, dar costisitoare, astfel încât în cazuri neclare, ecocardiografia transesofagiană este mai des utilizată.
Cateterismul și angiografia, precum și aortografia, sunt standardul de aur pentru diagnosticarea malformațiilor cardiace congenitale, dar sunt efectuate în spitale specializate de chirurgie cardiacă cel mai adesea ca ultima etapă diagnostic sau examen preoperator.
Metodele de clarificare a ultimei etape a diagnosticului CHD sunt ecocardiografia transesofagiană, rezonanța magnetică și tomografia computerizată multislice a inimii. Cateterismul și angiografia, inclusiv aortografia, sunt standardele de aur pentru diagnosticarea CHD.
malformatii frecvente cu care pacientii supravietuiesc pana la varsta adulta
malformații fără cianoză și șunt
Acest grup de defecte include: valva aortică bicuspidiană, coarctația aortei și stenoza valvei pulmonare.
Valva aortică bicuspidiană
O valvă aortică bicuspidiană este un defect destul de comun.
Într-o valvă aortică normală, există trei foițe de dimensiuni egale, adică. valva aortică normală este tricuspidiană. Folioarele sunt separate prin comisuri și sunt susținute de inelul fibros al valvei aortice. Toate cele trei valve sunt situate în sinusurile lui Valsalva (sinusurile coronare) - pliurile rădăcinii aortice, din care pleacă arterele coronare. Artera coronară dreaptă se îndepărtează de sinusul coronar drept, deci
numele sinusului; Artera coronară stângă ia naștere din sinusul coronar stâng. Arterele coronare nu se îndepărtează de al treilea sinus și se numește non-coronare. În consecință, aceste sinusuri sunt numite și foițe ale valvei aortice: folie coronară dreaptă, coronară stângă și folie necoronară a valvei aortice
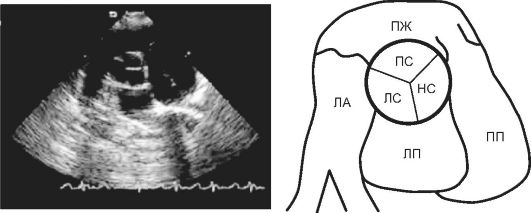 Orez. 11.2. Sistem. EchoCG transtoracic în modul B în poziția parasternală a axei scurte a valvei aortice tricuspide normale și schema acesteia (LA - atriul stâng, LA - atriul drept, RV - ventricul drept, LA - artera pulmonară, LS - cuspid coronar stâng al valvei aortice, PS - cuspid coronar drept al acesteia, NS - cuspid non-coronar)
Orez. 11.2. Sistem. EchoCG transtoracic în modul B în poziția parasternală a axei scurte a valvei aortice tricuspide normale și schema acesteia (LA - atriul stâng, LA - atriul drept, RV - ventricul drept, LA - artera pulmonară, LS - cuspid coronar stâng al valvei aortice, PS - cuspid coronar drept al acesteia, NS - cuspid non-coronar)
Într-o valvă aortică bicuspidiană există doar două foliole de dimensiuni aproape egale (Fig. 11.3). Valvele pot ocupa pozitia dreapta-stanga si anteroposterioara. În primul caz, există două sinusuri coronare, din care pleacă arterele coronare, în al doilea, ambele artere coronare pleacă din sinusul foliar anterior (V.I. Burakovsky et al., 1996).
Cel mai adesea, o valvă aortică bicuspidă este detectată incidental în timpul ecocardiografiei. Astfel de pacienți se simt bine, nu au simptome. Pericolul unei valve bicuspidiene este că fibroza și calcificarea se dezvoltă în ea mai des decât într-o valvă tricuspidă. Ca urmare, până la vârsta de 50-60 de ani sau mai devreme, se formează stenoza secțiunii de evacuare a orificiului aortic și apare un defect hemodinamic semnificativ. Și adesea se schimbă
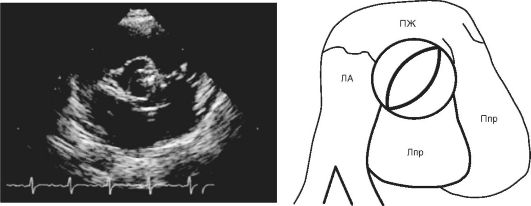 Orez. 11.3. Sistem. Ecocardiografia transtoracică în modul B în poziția parasternală a axei scurte a valvei aortice bicuspide și schema acesteia (notația este aceeași ca în Fig. 11.2)
Orez. 11.3. Sistem. Ecocardiografia transtoracică în modul B în poziția parasternală a axei scurte a valvei aortice bicuspide și schema acesteia (notația este aceeași ca în Fig. 11.2)
Diferențele sunt atât de mari încât în timpul operației chirurgul nu poate spune dacă această valvă a fost inițial bicuspidă sau tricuspidă. În alte cazuri, degenerarea valvei bicuspide se dezvoltă rapid, ducând la insuficiența acesteia. Uneori, valva aortică este stenotică imediat după nașterea unui copil din cauza fuziunii comisurilor sale sau a displaziei sale.
Trebuie amintit că valva aortică bicuspidă este adesea asociată cu alte boli congenitale, în primul rând cu coarctația aortei. Prin urmare, prezența unei valve aortice bicuspide necesită o examinare obligatorie a pacientului pentru a exclude coarctația aortei - măsurarea presiunii asupra picioarelor, ceea ce, din păcate, adesea nu se face. De asemenea, este important ca la o valvă aortică bicuspidă să existe o anomalie a țesutului mezenchimal, prin urmare, cu acest defect, frecvența disecțiilor aortice este crescută. Pacienții cu valvă aortică bicuspidă sunt expuși riscului de endocardită infecțioasă și necesită profilaxia acesteia. Chirurgia cardiacă este necesară la pacienții care au sau au dezvoltat stenoză și/sau insuficiență a valvei aortice semnificative hemodinamic.
Valva aortică bicuspidă este o malformație frecventă cu dezvoltarea fibrozei și calcifierii valvulare, cu risc crescut de endocardită infecțioasă și disecție aortică.
Coarctația aortei
Coarctarea aortei este îngustarea sa segmentară congenitală. Cel mai adesea, coarctația are loc la joncțiunea arcului aortic cu partea sa descendentă - în zona istmului său, distal de artera subclavie stângă. Îngustarea poate fi localizată proximal de confluența canalului arterios deschis (OAP) - variantă preductală și distal de PDA - variantă postductală a coarctației aortice (Fig. 11.4 A și B). Uneori, îngustarea este situată direct la confluența PDA în aortă - coarctația juxtaductală. Contractia poate reprezenta
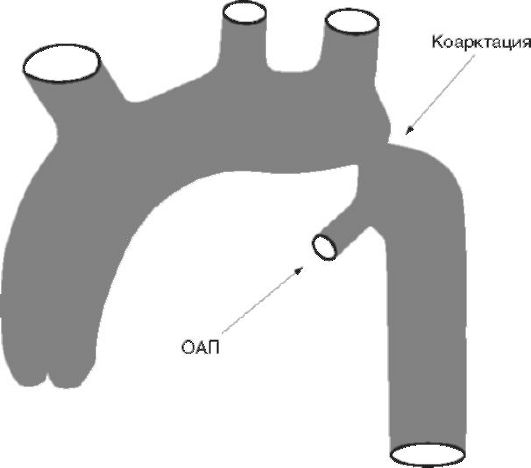 Orez. 11,4 A. Schema coarctației preductale a aortei. Îngustarea este situată proximal de canalul arterial permeabil (PDA)
Orez. 11,4 A. Schema coarctației preductale a aortei. Îngustarea este situată proximal de canalul arterial permeabil (PDA)
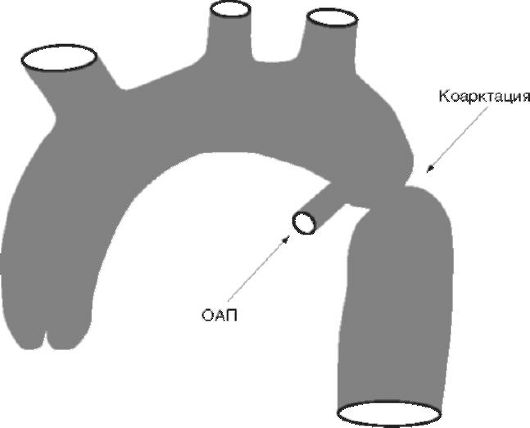 Orez. 11.4 B. Schema coarctației postductale a aortei. Îngustarea este situată distal de canalul arterial permeabil (PDA)
Orez. 11.4 B. Schema coarctației postductale a aortei. Îngustarea este situată distal de canalul arterial permeabil (PDA)
o diafragmă cu o gaură sau un pliu în formă de semilună în lumenul aortei sau, care apare în varianta preductală, îngustarea difuză a întregului istm al aortei și, uneori, arcada acestuia. Aorta post-stenotică se poate dilata și subțire din cauza expunerii constante la fluxul sanguin turbulent.
Există trei variante clinice de coarctație aortică: I - coarctație izolată; II - coarctația aortei în combinație cu PDA; III - coarctație în combinație cu alte CHD (A.V. Pokrovsky, 1979). IN SI. Burakovsky și colab., în plus, evidențiază o variantă în care coarctația este combinată cu un defect IVS (1996).
Când diametrul stenozei este cu 1/3 mai mic decât în mod normal, se produce o cădere de presiune (gradient). Acest lucru duce la faptul că în circulația sistemică se creează două moduri de circulație a sângelui: proximal de stenoză, apare tensiunea arterială mare și fluxul sanguin ridicat, iar mai jos, presiunea scăzută și fluxul sanguin scăzut. Pentru a depăși acest lucru, încep să funcționeze numeroase colaterale, la care participă arterele subclavie, arterele intratoracice, arterele intercostale (cu excepția primelor două perechi), vase din jurul scapulei, artera epigastrică superioară, arterele spinale anterioare și vertebrale. Atunci când este combinat cu un PDA, descărcarea prin acesta este mult mai mare decât în cazul unui canal deschis izolat, ceea ce crește semnificativ fluxul sanguin pulmonar și afluxul către inima stângă.
Modificările inimii apar deja în uter - hipertrofiile ventriculului drept, tk. lucrează împotriva rezistenței crescute a cercului mare. După nașterea unui copil, natura fluxului sanguin se modifică și apare hipertrofia ventriculului stâng al inimii, deoarece. acum funcționează împotriva rezistenței crescute. O astfel de hipertrofie nu este însoțită de o creștere a fluxului sanguin în ventriculul stâng, care la unii pacienți duce la dezvoltarea fibroelastozei miocardice.
În cursul clinic al defectului, se disting mai multe perioade:
primul- primul an de viață: în această perioadă pot apărea primele manifestări severe ale defectului, iar practic se decide dacă copilul va trăi;
Dacă copilul supraviețuiește primei menstruații, atunci a doua perioada care acoperă vârsta de la 1 la 5 ani - perioadă
adaptări, caracterizate în principal prin manifestări ușoare ale sindromului de hipertensiune arterială sau absența completă a simptomelor;
al treilea- pana la 14 ani - pubertate - perioada de compensare - absenta completa a simptomelor;
A patra perioadă (vârsta 15-20 ani) este decompensarea relativă, apar simptome clinice;
A cincea perioadă este perioada de decompensare.
Tabloul clinic al coarctației aortei la adulți constă din trei grupuri de plângeri:
1. plângeri asociate cu prezența sindromului de hipertensiune arterială ( durere de cap, sângerări nazale etc.);
2. Reclamații datorate muncă sporită VS (durere în piept, insuficiență cardiacă etc.);
3. plângeri asociate cu scăderea fluxului sanguin în jumătatea inferioară a corpului (oboseală și durere la nivelul picioarelor, oboseală rapidă etc.).
Pacienții sunt de obicei bine dezvoltați fizic, la unii pacienți există o disproporție între dezvoltarea musculară a centurii superioare și inferioare. La examinare, puteți vedea pulsația vaselor gâtului, uneori - arterele intercostale.
În timpul auscultației, se aude un suflu sistolic la vârful și baza inimii, uneori pe spate, între omoplați. Atunci când sunt combinate cu alte defecte, poate exista un tablou auscultator mai complex. Al doilea ton pe aortă este crescut. La unii pacienți se poate auzi un zgomot continuu de circulație colaterală în regiunea interscapulară.
Diagnosticul acestui defect este relativ simplu: identificarea de mare tensiune arteriala când se măsoară pe arterele brahiale şi presiune scăzută pe arterele picioarelor la pacienții tineri sugerează coarctarea aortei (la persoanele sănătoase, tensiunea arterială este cu 10-15 mm Hg mai mare pe picioare decât pe brațe). Examinarea cu raze X relevă uzura coastei, care este asociată cu o creștere a diametrului arterelor intercostale, ceea ce duce la dezvoltarea osteoporozei coastelor, o creștere a ventriculului stâng și, uneori, a atriului stâng. Cu ecocardiografia în modul B, se poate observa un istm stenotic al aortei din abord suprasternal. Diagnosticul este confirmat prin ecocardiografie transesofagiană sau imagistică prin rezonanță magnetică.
Fără tratament, majoritatea pacienților cu coarctație a aortei care au supraviețuit până la vârsta adultă mor la vârsta de 20-50 de ani, 70% dintre pacienți nu trăiesc până la 40 de ani. Principalele cauze de deces sunt decompensarea, ruptura anevrismelor aortei și a altor vase, anevrismele disecante ale aortei și endocardita infecțioasă.
Chirurgia cardiacă este mai des efectuată în copilărie. La pacienții adulți, totul depinde de absența sau prezența hipertensiunii pulmonare persistente, decompensarea severă etc.
Coarctarea aortei reprezintă îngustarea sa segmentară congenitală.
În același timp, în circulația sistemică sunt create două moduri de flux sanguin: hipertensiunea arterială și fluxul sanguin ridicat apar proximal de stenoză și dedesubt. - tensiune arterială scăzută și flux sanguin scăzut.
Stenoza valvulară pulmonară izolată (ISLA)
Acesta este un defect destul de comun (aproximativ 10% din totalul CHD). Constă în prezența fuziunii cuspidelor valvei trunchiului pulmonar, din cauza căreia există un obstacol în calea mișcării sângelui - o scădere a presiunii peste valvă. Cel mai adesea, supapele sunt topite și formează o diafragmă membranoasă cu o deschidere rotundă sau ovală. O astfel de membrană în sistola ventriculului drept al inimii se îndoaie în lumenul arterei pulmonare, în diastolă - există chiar și o anumită deviație către ventriculul drept al inimii. Speranța de viață a pacienților depinde în mare măsură de dimensiunea acestei găuri - dacă diametrul său este mai mare de 1 cm, atunci cursul defectului poate fi favorabil, iar pacienții trăiesc până la vârsta adultă.
Obstrucția fluxului de ieșire din ventriculul drept al inimii duce la o creștere semnificativă a presiunii - presiunea sistolica în acesta poate ajunge la 200 mm Hg, în timp ce presiunea în artera pulmonară rămâne normală sau chiar oarecum redusă. Munca ventriculului drept pentru a depăși stenoza duce la apariția unei hipertrofii semnificative a miocardului secțiunii sale de ieșire și, în cazuri severe, la fibroză endocardică.
Principala plângere a pacienților cu ISLA este dispneea la efort, iar la unii pacienți chiar în repaus. Unii pacienți experimentează durere în regiunea inimii asociată cu
insuficiență coronariană severă într-un ventricul drept hipertrofiat. Cianoza nu este caracteristică ISLA, cu excepția cazurilor de insuficiență ventriculară dreaptă severă cu foramen oval permeabil. La astfel de pacienți, presiunea în atriul drept crește, iar când foramenul oval este deschis, apare o descărcare din atriul drept spre stânga, ceea ce duce la apariția cianozei. Cu o dilatare mare a ventriculului drept al inimii, poate apărea o „cocoașă a inimii”, o pulsație a venelor gâtului. Palparea toracelui evidențiază tremor sistolic.
În timpul auscultării în spațiul intercostal II-III din stânga sternului, se aude un suflu sistolic aspru, care este condus la claviculă stângă, tonul I este crescut (poate fi slăbit în timpul decompensării), tonul II este slăbit. sau dispare. La unii pacienți cu ISLA se aude un suflu moale protodiastolic al insuficienței valvei pulmonare.
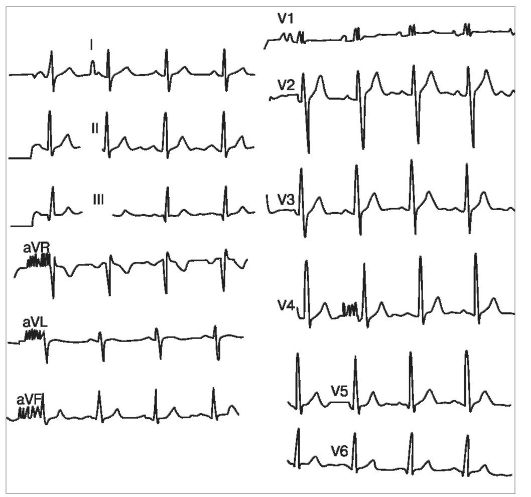 Orez. 11.5. ECG al unui pacient cu stenoză pulmonară moderată. Pozitie verticala axa electrică a inimii, blocarea incompletă a ramurii drepte a fasciculului de His
Orez. 11.5. ECG al unui pacient cu stenoză pulmonară moderată. Pozitie verticala axa electrică a inimii, blocarea incompletă a ramurii drepte a fasciculului de His
ECG prezintă de obicei semne de supraîncărcare atrială dreaptă și hipertrofie ventriculară dreaptă (Fig. 11.5).
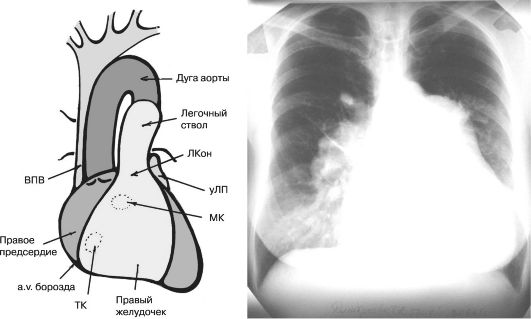
Radiografia în poziție anteroposterior evidențiază o proeminență post-stenotică a arcului arterei pulmonare și un model pulmonar normal sau epuizat (Fig. 11.6.) Și o creștere a atriului drept.
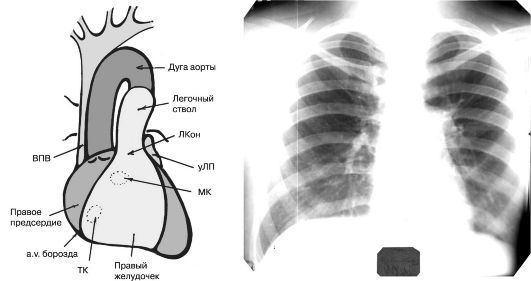 Orez. 11.6. Radiografia unui pacient cu stenoză moderată a arterei pulmonare și o diagramă a proiecției camerelor inimii și a vaselor mari în proiecția anteroposterioră (SVC - vena cavă superioară, LA - apendice atrial stâng, LCA - con pulmonar, MK - valva mitrala, TC - valva tricuspidiana). Model pulmonar oarecum epuizat, proeminență post-stenotică a arcului arterei pulmonare
Orez. 11.6. Radiografia unui pacient cu stenoză moderată a arterei pulmonare și o diagramă a proiecției camerelor inimii și a vaselor mari în proiecția anteroposterioră (SVC - vena cavă superioară, LA - apendice atrial stâng, LCA - con pulmonar, MK - valva mitrala, TC - valva tricuspidiana). Model pulmonar oarecum epuizat, proeminență post-stenotică a arcului arterei pulmonare
Cu ecocardiografie, este posibil să se vizualizeze hipertrofia și dilatarea semnificativă a ventriculului drept al inimii (Fig. 11.7, vezi insert), precum și cuspizii valvei pulmonare care formează membrana (Fig. 11.8, vezi insert). ). Cu ecocardiografia Doppler color, turbulența este vizibilă pe valvă, când este măsurată cu Doppler cu undă continuă, este vizibil un gradient de presiune (Fig. 11.9, vezi insert).
Diagnosticul final este confirmat prin sondare și examen angiografic. Chirurgia cardiacă este indicată pentru toți pacienții cu stenoză valvulară pulmonară severă și severă (presiunea sistolica în ventriculul drept este mai mare).
61 mm Hg). Pentru pacienții cu decompensare, tratamentul chirurgical se efectuează după eliminarea acestuia. Pacienții cu stenoză moderată ar trebui să fie sub supravegherea constantă a unui cardiolog și a unui chirurg cardiac.
ISLA reprezintă cel mai adesea fuziunea cuspidelor valvelor trunchiului pulmonar sub formă de membrană, din cauza căreia există o obstrucție a mișcării sângelui și o scădere a presiunii.
malformații fără cianoză cu șunt stânga-dreapta
Un alt grup de malformații comune cu care pacienții pot supraviețui până la vârsta adultă includ defectul septal atrial (ASD) de tipul ostium secundum, canal arterial (botalian) deschis, defect restrictiv al IVS.
Defect MPP
tip DMPPostium secundum
Un defect este o gaură (mesaj) în MPP prin care sângele este evacuat. Poate fi localizat oriunde: central, proximal - aproape de orificiile venelor pulmonare, la mijlocul septului, la orificiul venei cave superioare. În același timp, partea de sept adiacentă direct valvelor atrioventriculare rămâne intactă. Evacuarea sângelui se efectuează de la stânga la dreapta, deoarece presiunea in atriul stang cu 3-5 mm Hg. mai sus decât în dreapta. Amploarea resetarii depinde de dimensiunea defectului, cu defecte mari, raportul de rezistență în găurile atrioventriculare, complianța ventriculară joacă, de asemenea, un rol.
Defectul se numește secundar (ostium secundum) deoarece provine din septul secundar. În embriogeneză, sunt depuse două septuri interatriale: primare și secundare. Secundarul este așezat la nivelul bazei inimii și în procesul de embriogeneză începe să se deplaseze caudal către deschiderile atrioventriculare. La nivelul valvelor atrioventriculare ia naștere septul primar interatrial care se deplasează spre baza inimii. Ambele partiții în procesul de embriogeneză sunt conectate în regiunea fosei ovale, creând acolo
un fel de duplicare, care formează o fosă ovală și devine valva ferestrei ovale.
Astfel, ASD care apar în septul secundar nu intră în contact cu valvele atrioventriculare. Adesea sunt adiacente gurii venelor pulmonare, iar apoi sângele din venele pulmonare intră direct în atriul stâng. În acest caz, se vorbește despre un defect secundar al MPP, combinat cu drenajul anormal al venelor pulmonare.
Boala poate progresa pentru o lungă perioadă de timp asimptomatică. Cu TSA mari situate în apropierea gurii venei cave, o cantitate mică de sânge venos poate fi aruncată în atriul stâng, ceea ce duce la hipoxemie ușoară și cianoză moderată. Odată cu decompensarea, apar simptome de insuficiență cardiacă de severitate diferită.
Auscultarea dezvăluie (adesea întâmplător) un suflu sistolic peste inimă. Zgomotul se aude în spațiul intercostal I-III din stânga sternului. Este un zgomot funcțional tipic și are un timbru de suflare, deși poate fi destul de puternic. Zgomotul apare deoarece, pe lângă volumul normal de sânge care intră în atriul drept și apoi în ventriculul drept din vena cavă, prin defect se adaugă sânge din atriul stâng. Prin urmare, volumul de sânge în ventriculul drept devine prea mare chiar și pentru o secțiune normală de ieșire, se creează o stenoză relativă a valvei pulmonare, ceea ce duce la apariția unui suflu sistolic.
În plus, un volum mare duce la dilatarea ventriculului drept, remodelarea acestuia. În acest caz, mușchii papilari ai valvei tricuspide se îndepărtează de inelul fibros și nu permit închiderea completă a valvelor, ceea ce duce la apariția regurgitației tricuspide. De asemenea, provoacă dilatarea inelului valvei tricuspidiene, care menține regurgitarea tricuspidiană. Toate acestea duc la un suflu sistolic destul de puternic. Acest zgomot poate trece prin întreaga sistolă și uneori, cu defecte severe, chiar trece prin componenta aortică a celui de-al doilea ton. În plus, se ascultă divizarea tonului II.
Pe ECG-ul pacienților cu TSA, consecințele supraîncărcării de volum a secțiunilor drepte sunt clar vizibile (Fig. 11.10). Pe ECG prezentat - poziția verticală a axei electrice a inimii. Se poate observa că
zona de intrare s-a mutat la stânga conducătorilor din dreapta, iar cei 5 dinți trece la V;Și V6; mare R V V1, V aVR- prong târzie R. Caracteristica acestui defect este o creștere a amplitudinii și ascuțirea undei P, faza sa negativă dispare în V1. La unii pacienți adulți cu TSA, fibrilația atrială este posibilă.
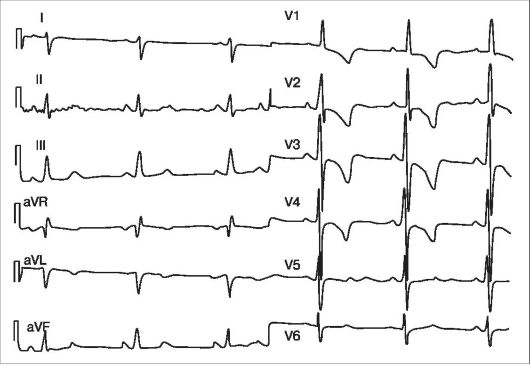 Orez. 11.10. ECG al unui pacient cu TSA secundar. Poziția verticală a axei electrice a inimii, semne de hipertrofie miocardică a ventriculului drept (SV profund 5-6), hipertrofie IVS (RV1 înalt)
Orez. 11.10. ECG al unui pacient cu TSA secundar. Poziția verticală a axei electrice a inimii, semne de hipertrofie miocardică a ventriculului drept (SV profund 5-6), hipertrofie IVS (RV1 înalt)
La examenul fluoroscopic, un semn caracteristic al TSA este „pulsația rădăcinilor” plămânilor. Pe radiografie în proiecția anteroposterioră se reduce o creștere a modelului pulmonar, o bombare a arcului arterei pulmonare și umbra aortei (Fig. 11.11). Odată cu decompensare, atriul drept crește semnificativ, ramura dreaptă a arterei pulmonare se extinde (Fig. 11.12).
Ecocardiografia poate dezvălui defectul în sine, care se va manifesta ca o întrerupere a semnalului de la MPP (Fig. 11.13, vezi insert). Pe ecocardiograma prezentată, defectul MPP este clar vizibil. Acesta este un defect secundar, deoarece o parte a septului primar este păstrată, adică MPP-ul la nivelul valvelor atrioventriculare este conectat. Când se aplică un raster Doppler color pe locul septului, este vizibilă o scurgere de sânge de la stânga la dreapta (Fig. 11.14, vezi insertul).
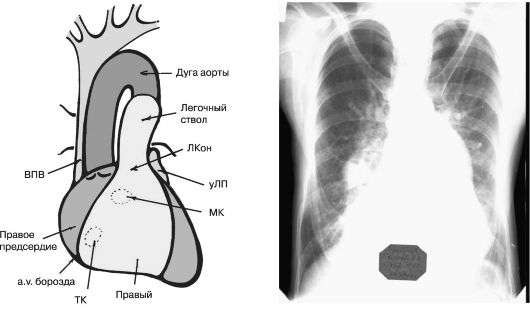
Orez. 11.11. Raze X în proiecția anteroposterioră a unui pacient cu TSA secundar și o diagramă a proiecției camerelor inimii și a vaselor mari (denumirile sunt aceleași ca în Fig. 11.6). Modelul pulmonar este îmbunătățit, arcul arterei pulmonare se umflă, umbra aortei este redusă
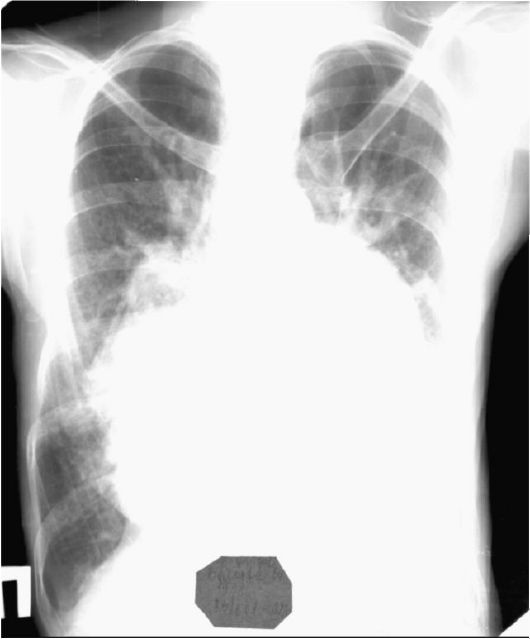 Orez. 11.12. Radiografie în proiecția anteroposterioră a aceluiași pacient după 2 ani, decompensare. Bombarea arcului arterei pulmonare a crescut semnificativ, atriul drept și ramura dreaptă a arterei pulmonare s-au extins
Orez. 11.12. Radiografie în proiecția anteroposterioră a aceluiași pacient după 2 ani, decompensare. Bombarea arcului arterei pulmonare a crescut semnificativ, atriul drept și ramura dreaptă a arterei pulmonare s-au extins
Cu toate acestea, examinarea transtoracică a MPP nu este întotdeauna clar vizibilă. Când se examinează inima în modul B în poziția apicală cu patru camere, uneori, la persoanele sănătoase, există o întrerupere a semnalului pe septul interatrial, deoarece fasciculul de ultrasunete în astfel de cazuri merge paralel cu septul interatrial și în unele cicluri. începe să se îndepărteze de grindă. Pentru a evita eroarea, pe lângă trimiterea pacientului către o ecocardiogramă transesofagiană, puteți încerca să efectuați un studiu din accesul epigastric (Fig. 11.15, vezi insert). În acest caz, MPP cade sub fasciculul ultrasonic perpendicular pe acesta, iar defectul este clar vizibil. La aplicarea clopotului color doppler, fluxul turbulent prin acest defect este clar vizibil.
Cateterismul cardiac poate confirma în mod fiabil prezența ASD. Semnul său principal va fi trecerea cateterului din atriul stâng spre dreapta și o creștere a saturației de oxigen din sânge în atriul drept în comparație cu cea din vena cavă.
Tratamentul TSA este chirurgia cardiacă. Fie defectul este suturat (mai puțin de 3 cm în diametru), fie septul este reparat cu un plasture de autopericard sau țesut sintetic. Pacienții cu un stadiu asimptomatic de TSA și presiune arterială pulmonară normală și dimensiunea inimii, care, în ciuda defectului, rămân apți de muncă, nu sunt supuși unei intervenții chirurgicale cardiace și anumit timp poate fi observată de către un cardiolog și un chirurg cardiac.
Așa-numitul TSA secundar este însoțit de o scurgere din atriul stâng spre dreapta și de un suflu sistolic peste inimă.
Sindromul Lutembashe (Lutembacher)
Sindromul Lutembashe este o combinație de TSA cu stenoză congenitală sau dobândită a orificiului atrioventricular stâng. Prezența stenozei mitrale crește șuntarea sângelui printr-un ASD. Simptomele clinice și auscultatorii depind de severitatea ambelor defecte. Metoda de diagnostic primar este ecocardiografia.
Reflex și sindromul Eisenmenger
După cum sa menționat deja, la pacienții cu TSA, fluxul sanguin pulmonar este crescut. În același timp, o creștere a volumului fluxului sanguin pulmonar nu duce la hipertensiune pulmonară ridicată, deoarece cel mai adesea rezistența vasculară pulmonară nu crește până la un anumit punct. Apoi, există un spasm al arteriolelor pulmonare - o reacție care vizează limitarea fluxului sanguin pulmonar. Crește treptat rezistența vasculară pulmonară. Acest fenomen se numește reflexul Eisenmenger. La pacienții adulți, spasmul arteriolelor pulmonare este înlocuit cu obstrucția lor organică persistentă, șuntul de la dreapta la stânga crește din ce în ce mai mult. O astfel de creștere persistentă a rezistenței vasculare pulmonare, apariția hipertensiunii pulmonare persistente ridicate și, ca urmare, o schimbare a direcției fluxului sanguin în malformații cu flux sanguin pulmonar crescut se numește sindromul Eisenmenger. Reflexul Eisenmenger apare cu malformații congenitale cu o scurgere mare de sânge de la stânga la dreapta: cu orice tip de TSA, duct arteriosus permeabil, defect septal ventricular și malformații congenitale mai complexe. Se manifestă prin apariția pe radiografie a semnelor unei scăderi a fluxului sanguin pulmonar și cel mai adesea aceasta înseamnă că îndepărtarea chirurgicală a unui TSA nu va duce la o scădere a presiunii în artera pulmonară și la eliminarea insuficienței ventriculare drepte. Astfel de pacienți sunt indicați pentru tratamentul terapeutic și/sau transplantul complexului inimă-plămân.
În prezent, pentru tratamentul terapeutic al pacienților cu sindrom Eisenmenger, pe lângă tratamentul simptomatic al insuficienței cardiace, corectarea eritrocitozei, manifestări hematologice secundare, cum ar fi deficitul de fier și tendința de tromboză, terapia intensivă cu analogi de prostaglandine, antagonistul endotelinei bosentan și/sau se recomandă sildenafilul antagonist al 5-fosfodiesterazei.
O creștere a tonusului arteriolelor pulmonare în CHD cu creșterea fluxului sanguin pulmonar se numește reflexul Eisenmenger. După dezvoltarea modificărilor morfologice la arteriole, rezistența vasculară pulmonară crește semnificativ, se dezvoltă hipertensiune pulmonară ridicată și, ca urmare, se modifică direcția fluxului sanguin, care se numește sindromul Eisenmenger.
Arteria deschisă (OAP) sau ductus arteriosus
PDA este un vas prin care se efectuează scurgerea patologică a sângelui din aortă în artera pulmonară. Canalul arterial funcționează în embriogeneză, conectând aorta și artera pulmonară. După nașterea unui copil, este ștearsă în 2-8 săptămâni.
Cel mai adesea, ductul pleacă din aortă la nivelul arterei subclaviei stângi și se varsă în trunchiul pulmonar la locul de bifurcare sau în artera pulmonară stângă (Fig. 11.16). PDA este acoperită de pleura parietală și pericard. Lungimea sa este de la 10 la 25 mm, lățimea - până la 20 mm.
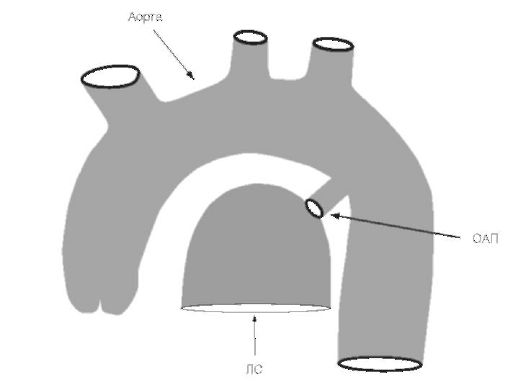 Orez. 11.16. Reprezentare schematică a canalului arterios deschis (PDA - ductus arteriosus deschis, LS - trunchiul pulmonar)
Orez. 11.16. Reprezentare schematică a canalului arterios deschis (PDA - ductus arteriosus deschis, LS - trunchiul pulmonar)
Deoarece presiunea în aortă este mai mare, șuntarea are loc de la aortă la artera pulmonară, apoi sângele oxigenat intră în plămâni, apoi în atriul stâng și în ventriculul stâng. În consecință, la astfel de pacienți, fluxul sanguin pulmonar a crescut și activitatea inimii stângi. Atriul stâng și ventriculul stâng se dilată și se hipertrofiază, iar aorta se extinde. Creșterea volumului de sânge care curge în secțiunile stângi poate fi atât de mare încât apare stenoza relativă a deschiderii atrioventriculare stângi. Odată cu adăugarea hipertensiunii pulmonare, ventriculul drept se hipertrofiază.
Speranța de viață a pacienților depinde de dimensiunea PDA. Dacă lumenul ductului este mic, hemodinamica se modifică lent. Astfel de pacienți pot trăi suficient de mult fără simptome.
Viciul poate să nu apară mult timp și se termină diagnostic tardiv, adesea când hipertensiunea pulmonară ireversibilă (reflexul Eisenmenger) a apărut deja. La unii pacienți, boala este complicată de endocardită infecțioasă; a fost descris și un anevrism al PDA, care se poate rupe. Sunt descrise cazuri izolate de închidere spontană a acestuia.
PDA în perioada asimptomatică poate fi detectată incidental în timpul auscultării inimii. În acest caz, se aude zgomotul caracteristic acestui defect special - așa-numitul suflu sistole-diastolic. Suflu aortic nu trebuie numit suflu sistolic-diastolic atunci când sunt prezente atât suflu sistolic, cât și proto-diastolic. Suflu sistolodiastolic se mai numește și suflu de mașină, deoarece poate fi destul de puternic, începe la mijlocul sistolei, trece prin al doilea ton și se termină în diastolă. Se aude bine în spațiul interscapular și pe vasele gâtului. Pe măsură ce se dezvoltă hipertensiunea pulmonară (sindromul Eisenmenger), intensitatea suflului scade, apoi componenta sa diastolică dispare și rămâne un suflu sistolic.
La examinare, uneori este detectată o „cocoașă a inimii”, o pulsație a toracelui în regiunea apexului. La palpare se evidențiază o creștere a bătăii apexului și tremur sistolic-diastolic sau sistolic.
Când apar simptomele, plângerile nu sunt specifice: apar slăbiciune, oboseală crescută.
Nu există modificări specifice la electrocardiograma pacienților cu PDA. Practic, sunt dezvăluite semne de hipertrofie și supraîncărcare a departamentelor corespunzătoare.
Examenul cu raze X relevă creșterea fluxului sanguin pulmonar (dacă nu există sindromul Eisenmenger), creșterea pulsației aortei dilatate și a arterei pulmonare, semne de creștere a secțiunilor stângi și, într-o anumită perioadă, a celor drepte.
Ecocardiografia și examinarea Doppler relevă flux turbulent în artera pulmonară stângă. Dacă se suspectează un canal arterios deschis, este mai bine să se efectueze un studiu din abord suprasternal (Fig. 11.17). Transductorul este aplicat pe fosa jugulară și se poate vedea o imagine a aortei. Sub ea este vizibil genunchiul arterei pulmonare stângi. Ele sunt conectate printr-un canal arterios deschis, iar prin plasarea unui clopot Doppler color, se poate vedea mișcarea turbulentă a sângelui.
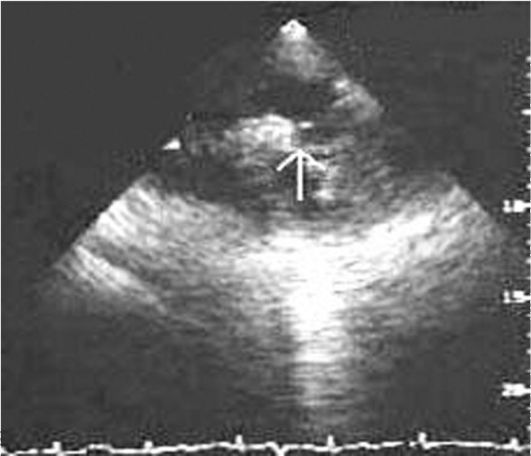 Orez. 11.17. EcoCG al canalului arterios deschis de la abordul suprasternal (indicat printr-o săgeată). Axul scurt la nivelul arcului aortic
Orez. 11.17. EcoCG al canalului arterios deschis de la abordul suprasternal (indicat printr-o săgeată). Axul scurt la nivelul arcului aortic
PDA este un vas prin care se efectuează scurgerea patologică a sângelui din aortă în artera pulmonară. Cel mai adesea, pleacă din aortă la nivelul arterei subclaviei stângi și se varsă în trunchiul pulmonar la locul de bifurcare sau în artera pulmonară stângă. Se caracterizează prin suflu sistolico-diastolic.
Defect restrictiv al părții musculare a septului interventricular
Un defect de sept ventricular (VSD) este o comunicare între ventriculii inimii la nivelul septului interventricular (VSD). Apare în embriogeneză fie din cauza creșterii insuficiente a componentelor IVS, fie din cauza lipsei conexiunii lor și este unul dintre cele mai frecvente defecte. VSD poate fi izolat și apare împreună cu alte anomalii congenitale, formând malformații congenitale complexe, complexe.
În prezent, în funcție de locația VSD-ului, există:
I. VSD perimembranoasă (perimembranoasă):
1) partea trabeculară;
2) intrare sau piesa de admisie;
3) ieșire sau parte de ieșire;
II. Defecte de flux subarterial.
III. Defecte musculare:
1) intrare sau piesa de admisie;
2) partea trabeculară;
3) ieșire sau parte de ieșire (V.I. Burakovsky și colab., 1996).
VSD restrictivă (boala Tolochinov-Roger) este un defect în care există un mic defect în VSD, mai mic de 1 cm (cel mai adesea în partea trabeculară sau perimembranoasă), pe care se creează o cădere mare de presiune (gradient) între ventricule. Cu VSD-uri mari, defectul în sine nu creează rezistență la fluxul de sânge prin sept, amploarea descărcării de la stânga la dreapta este determinată de diferența de rezistență în aortă și artera pulmonară, volumul de descărcare poate fi mare.
Într-un VSD restrictiv, rezistența la fluxul sanguin în sistolă este creată de defectul în sine, ca urmare a căruia există un gradient de presiune sistolică mare (aproximativ 100 mm Hg) și volumul de sânge care curge din stânga. ventriculul din dreapta este mic. Ca urmare, hemodinamica se modifică puțin - fluxul de sânge în plămâni și fluxul de intrare în părțile stângi ale inimii crește. Acest lucru provoacă suprasolicitarea lor și chiar hipertrofie moderată a VS.
Odată cu vârsta, acest defect se poate închide spontan datorită închiderii defectului de către valva tricuspidiană, datorită creșterii țesutului fibros, proliferării endocardului, închiderii marginilor defectului sau deveni mai mic în raport cu volumul în creștere. ale ventriculilor inimii.
Tabloul clinic constă în plângeri de palpitații, o scădere moderată a toleranței la efort și adesea VSD restrictivă este asimptomatică. Uneori există o mică „cocoașă a inimii”, palparea poate evidenția tremurături sistolice.
Auscultația evidențiază un suflu sistolic aspru, puternic în spațiul intercostal III-IV din stânga sternului, crescând spre stern. Intensitatea și timbrul zgomotului se explică prin faptul că defectul este mic, iar gradientul de presiune între stânga și
ventriculul drept este foarte mare, odată cu trecerea sângelui prin defect, apar turbulențe. Datorită faptului că defectul este adesea silențios din punct de vedere clinic și nu necesită tratament chirurgical, iar suflul sistolic este foarte puternic, acest defect este adesea denumit „mult zgomot pentru nimic”.
Pe electrocardiograma cu un VSD restrictiv, este posibil să nu existe nimic sau să apară semne de supraîncărcare a departamentelor din stânga.
Radiografic se poate detecta o ușoară creștere a inimii stângi, modelul pulmonar este normal.
Când se examinează un astfel de pacient folosind ecocardiografia în modul B, defectul poate fi vizualizat. Adesea, fluxul sanguin turbulent este detectat doar cu Doppler color.
Pacienții cu un astfel de defect nu sunt supuși unei intervenții chirurgicale cardiace. Trebuie să fie sub supravegherea unui cardiolog, observați măsuri preventiveîmpotriva endocarditei infecțioase.
Un VSD restrictiv este o comunicare anormală între ventriculii inimii. Cu un defect mai mic de 1 cm, volumul manevării este limitat.Defectul nu se manifestă adesea clinic și nu necesită tratament chirurgical.
malformații rare cu care pacienții supraviețuiesc până la vârsta adultă
malformații fără cianoză, fără șunt, cu leziuni ale inimii stângi
insuficiență mitrală congenitală
CHD, în care funcția obturatoare este afectată valva mitrala iar în sistolă, o parte din sângele din ventriculul stâng revine în atriul stâng. Cauzele insuficienței mitrale congenitale pot fi dilatarea inelului fibros al valvei mitrale, ceea ce face imposibilă contactul strâns cu foile în sistolă, scindarea foilor, anomalia coardelor valvei mitrale,
ceea ce duce la prolaps de foliole, defecte ale foliolei și diferite anomalii ale coardelor, mușchilor papilari și atașamentelor foliolei. Simptomele clinice, tabloul auscultator, datele metodelor instrumentale de cercetare sunt aceleași ca în insuficiența mitrală de altă etiologie. Pentru diagnostic diferenţial mare importanță atașat la datele anamnestice (detecția zgomotului și a altor semne de insuficiență mitrală din momentul nașterii sau din prima copilărie) și excluderea semnelor unui defect dobândit. Cu insuficiență mitrală congenitală semnificativă hemodinamic și tabloul clinic corespunzător - tratament chirurgical.
stenoză subaortică congenitală este un defect în care o obstrucție la ieșirea din ventriculul stâng este creată fie de o membrană circulară fibroasă, de un pliu fibros în formă de semilună, fie de un diafis fibromuscular limitat sau răspândit (stenoză fibromusculară). Membranele sunt atașate la un capăt de-a lungul septului interventricular sub inelul fibros al valvei aortice, iar la celălalt - la baza valvei mitrale. Cardiomiopatie obstructivă hipertrofică- Stenoza subaortică hipertrofică idiopatică nu se numără printre defectele de acest tip. Hemodinamica la pacienții cu astfel de defecte este modificată în același mod ca și în alte tipuri de stenoză aortică. Cel mai adesea, hipertrofia miocardică a VS se dezvoltă datorită activității sale crescute pentru a depăși stenoza, care este înlocuită de decompensarea acesteia. Din punct de vedere clinic, sunt detectate dificultăți de respirație, durere la inimă, amețeli și leșin. În spațiul intercostal II-III din stânga sternului se aude un suflu de ejecție. Diagnosticul diferenţial se realizează cu SA dobândită, coarctaţia aortei, stenoza arterei pulmonare, VSD, cu cardiomiopatie obstructivă. Metoda de diagnostic decisivă este ecocardiografia, care poate evidenția membrana și îngroșarea fibromusculară a peretelui și gradientul de presiune în secțiunea de evacuare a ventriculului stâng, precum și cateterismul cardiac. Lectură absolută un gradient de presiune mai mare de 80 mm Hg servește ca tratament chirurgical. În alte cazuri, se procedează de la severitatea simptomelor clinice.
malformații fără cianoză, fără șunt,
cu leziuni la partea dreaptă a inimii
Acest grup de malformații include anomalia Ebstein, anomalia Uhl, insuficiența valvei pulmonare (în formă izolată este extrem de rară, fără malformații concomitente, pacienții supraviețuiesc până la vârsta adultă fără simptome clinice, cu excepția suflului protodiastolic pe artera pulmonară), stenoze subvalvulare și supravalvulare ale artera pulmonară ( coarctația arterei pulmonare), dilatarea idiopatică a trunchiului arterei pulmonare.
anomalie Ebstein
Acesta este un defect, care este o anomalie a valvei tricuspide, în care foile sale nu sunt atașate de inelul fibros, ci sunt dispuse elicoidal de-a lungul suprafata interioara ventricul drept - fiecare frunză este atașată sub cea anterioară și se deplasează spre vârf. Folioul posterior este întotdeauna deplasat în cavitatea ventriculului drept și de multe ori foișorul septal, foioul anterior rămâne cel mai adesea la locul său obișnuit.
Se dezvoltă dilatarea atriului drept și a acelei părți a ventriculului drept care se află deasupra valvelor. Se numește partea dilatată a ventriculului drept, situată deasupra valvelor atrializat. Atriul drept cu această porțiune atrializată a ventriculului drept creează o formare de cavitate mare. Sub valve se află o mică parte a ventriculului drept funcțional. Se dezvoltă dilatarea severă a inelului fibros al valvei tricuspidiene și regurgitarea tricuspidiană.
Pe lângă atașarea necorespunzătoare, sunt adesea detectate anomalii ale valvei tricuspide - acestea pot fi răspândite de-a lungul pereților, de exemplu, cuspidul septal de-a lungul IVS. Distopiile foliare și anomaliile acestora pot duce la stenoza orificiului atrioventricular drept sau la stenoza tractului de evacuare din ventriculul drept.
Hemodinamica defectului constă într-o scădere semnificativă a ejecției din ventriculul drept al inimii și prin reducerea camerei de funcționare a acesteia și prin reducerea afluxului în acesta. Fluxul de intrare în ventriculul drept este redus datorită faptului că depolarizarea părții sale atrializate are loc concomitent cu cea distală, care
duce la faptul că, în momentul sistolei atriului drept, partea atrializată a camerei este în faza de diastolă, iar sângele curge slab din atriu în ea. În prezența stenozei orificiului atrioventricular drept, fluxul de sânge către ventriculul drept este redus și mai mult. O scădere a volumului vascular cerebral al ventriculului drept duce la o scădere a fluxului sanguin pulmonar.
Dilatarea atriului drept nu poate continua la infinit și, în cele din urmă, presiunea din acesta crește semnificativ și apare stagnarea în venele cercului mare.
Tabloul clinic depinde de severitatea tulburărilor hemodinamice. Majoritatea pacienților trăiesc până la 20-30 de ani, unii până la 40 și 50 de ani. Pacienții se plâng cel mai adesea de dificultăți de respirație, palpitații, oboseală și durere în regiunea inimii. Dacă există un mesaj între atriul drept și cel stâng (foramen oval deschis asociat cu ASD), poate apărea cianoză. Acrocianoza este posibilă și datorită debitului cardiac scăzut. Prezența unei camere mari a inimii, care este reprezentată de atriul drept și partea atrială a ventriculului drept, duce la apariția unei „cocoașe de inimă”. În stadiul de decompensare, există umflarea venelor gâtului, mărirea ficatului, splina, apariția sindromului hemoragic din cauza hipersplenismului.
La ascultarea unor astfel de pacienți, se evidențiază o slăbire a zgomotelor inimii, diferite ritmuri de galop, un murmur moale de insuficiență tricuspidiană în spațiul IV intercostal parasternal la stânga.
Pe ECG (Fig. 11.18), este crescută amplitudinea undei P, care în derivația II și în piept drept. (V) depaseste amplitudinea QRS- complex. Posibilă blocare a ramului drept al fasciculului His, tulburări de ritm, sindrom Wolff-Parkinson-White.
Radiografia anteroposterior evidențiază o transparență pulmonară crescută și cardiomegalie marcată cu umbră sferică a inimii datorită creșterii atriului drept (Fig. 11.19). Destul de des arcul unei artere pulmonare dispare.
EchoCG (Fig. 11.20) relevă atașarea incorectă a foișoarelor valvei tricuspide și deplasarea ei în ansamblu spre apex, o modificare a mișcării foilor și anomaliile acestora.
Diagnosticul este confirmat prin cateterism cardiac.
Diagnosticul diferențial la pacienții adulți se realizează cu cardiomiopatie, cu alte defecte cardiace congenitale și dobândite. Am observat un pacient care fusese
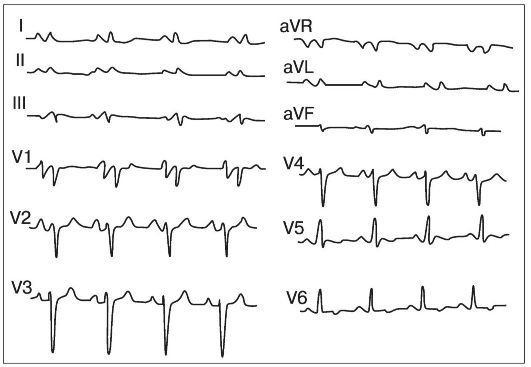 Orez. 11.18. ECG al unui pacient cu anomalie Ebstein. Amplitudinea undelor P este semnificativ crescută, ceea ce în V 1 depășește amplitudinea complexului QRS
Orez. 11.18. ECG al unui pacient cu anomalie Ebstein. Amplitudinea undelor P este semnificativ crescută, ceea ce în V 1 depășește amplitudinea complexului QRS
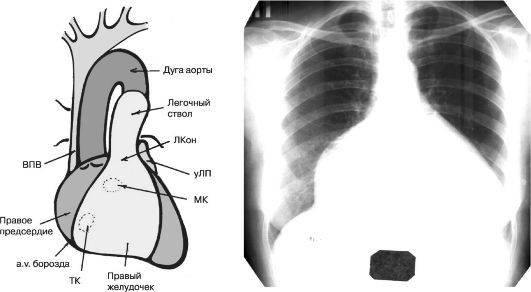 Orez. 11.19. Raze X în proiecția anteroposterioră a unui pacient cu anomalie Ebstein. Transparența plămânilor este crescută, cardiomegalia cu o umbră sferică a inimii datorită creșterii atriului drept, arcul arterei pulmonare este netezit
Orez. 11.19. Raze X în proiecția anteroposterioră a unui pacient cu anomalie Ebstein. Transparența plămânilor este crescută, cardiomegalia cu o umbră sferică a inimii datorită creșterii atriului drept, arcul arterei pulmonare este netezit
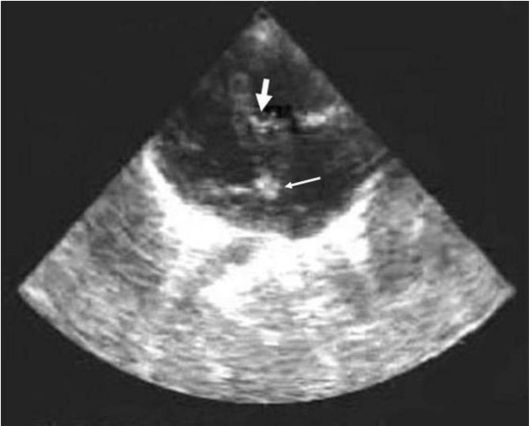 Orez. 11.20. Ecocardiografia unui pacient cu anomalie Ebstein în modul B. Poziția subcostală a axei lungi a inimii. Se observă atașarea incorectă a foiței septale a valvei tricuspide (săgeata groasă, săgeata subțire indică inelul valvei tricuspidiene)
Orez. 11.20. Ecocardiografia unui pacient cu anomalie Ebstein în modul B. Poziția subcostală a axei lungi a inimii. Se observă atașarea incorectă a foiței septale a valvei tricuspide (săgeata groasă, săgeata subțire indică inelul valvei tricuspidiene)
s-a pus diagnosticul de stenoză reumatică a orificiului atrioventricular stâng.
Tratamentul cardiochirurgical crește cu adevărat speranța de viață a acestor pacienți. De aceea diagnostic în timp util iar trimiterea către un chirurg cardiac pentru pacienții cu anomalie Ebstein este esențială. În prezent, se folosesc două tipuri de operații: reconstrucția plastică a valvei tricuspide și înlocuirea acesteia cu una artificială.
Anomalia lui Ebstein este un defect al valvei tricuspide, în care foliolele sale nu sunt atașate de inelul fibros, ci sunt dispuse elicoidal de-a lungul suprafeței interioare a ventriculului drept - fiecare foliolă este atașată sub cea anterioară și se deplasează către apex.
Anomalia lui Ul
Anomalia lui Ul- un fel de hipoplazie sau aplazie a miocardului ventriculului drept, până la dispariția completă a acestuia. Acest lucru duce la dilatarea acestuia, subțierea peretelui, motiv pentru care boala este numită și „ventricul drept pergament”. Unii pacienți dezvoltă insuficiență ventriculară dreaptă, în timp ce alții nu o dezvoltă și supraviețuiesc până la vârsta adultă. Anomalia lui Uhl este descrisă la un bărbat de 80 de ani. Aceasta este o anomalie destul de rară. Ventriculul drept practic nu se contractă, iar sângele este împins în principal de atriul drept. Diagnosticul se pune prin ecocardiografie. La vârsta adultă, boala poate să nu difere de cardiomiopatia ventriculară dreaptă aritmogenă.
malformații fără cianoză, cu șunt stânga-dreapta
TSA primar
ASD tip ostium primum, sau TSA primar; confluența parțială anormală a venelor pulmonare în atriul drept sau vena cavă; anevrism congenital al sinusului Valsalva; fistule coronare arteriovenoase. Ultimul defect este diagnosticat extrem de rar.
TSA primar cel mai adesea găsit ca parte a unui alt defect, care este o combinație de anomalii intracardiace - un canal atrioventricular deschis (AVK). Cu OAVK, principalele modificări apar la joncțiunea părții membranoase a IVS și ISP primar.
Într-o inimă formată în mod normal, ambele partiții sunt conectate în regiunea așa-numitei partiții intermediare. Inelul valvei tricuspide este situat deasupra inelului valvei mitrale, iar „septul intermediar” separă atriul drept de ventriculul stâng. Cu OAVK, nu există sept intermediar și MPP primar conectat la acesta într-o inimă normală, precum și secțiunea de intrare a IVS. Ca rezultat, se formează un defect comun în centrul inimii (V.I. Burakovsky și colab., 1996). Valvele atrioventriculare sunt la același nivel, foița mitrală anterioară are contact direct cu foița septală a valvei tricuspide, aceste foițe sunt
sunt despicate, există un inel fibros comun al valvelor atrioventriculare, foișoarele nu sunt atașate la IVS (sau sunt atașate parțial de acesta) și traversează defectul de fapt sub forma unui singur foișor.
La plin canal atrioventricular cel mai adesea, copiii fără tratament chirurgical nu sunt viabili și mor vârstă fragedă până la sfârșitul primului an de viață.
ASD primar este o variantă a OAVK parțială și este adesea asociată cu despicarea foiței mitrale și, uneori, a foiței septale a valvei tricuspide. Cu TSA primar, pacienții supraviețuiesc până la vârsta adultă.
Modificări hemodinamice şi tablou clinic va depinde de magnitudinea TSA și insuficiența valvei mitrale. În timpul auscultării în spațiul II intercostal din stânga sternului se determină un suflu sistolic caracteristic TSA, deasupra apexului - un suflu de regurgitare mitrală.
Pe ECG (Fig. 11.21) - abaterea axei electrice a inimii spre stânga, semne de hipertrofie a ventriculului drept (sau ambelor), atriul drept.
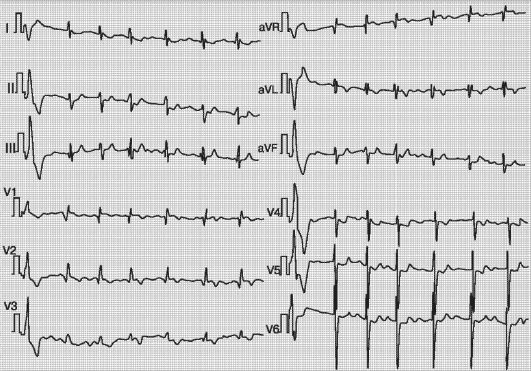 Orez. 11.21. ECG al unui pacient cu TSA primar. Fibrilatie atriala. Semne de hipertrofie severă și supraîncărcare a ventriculului drept al inimii (ECG de tip S, profund S V56, mare R Vl _ 2)
Orez. 11.21. ECG al unui pacient cu TSA primar. Fibrilatie atriala. Semne de hipertrofie severă și supraîncărcare a ventriculului drept al inimii (ECG de tip S, profund S V56, mare R Vl _ 2)
Pe radiografie în proiecția anteroposterioră (Fig. 11.22), se evidențiază un model pulmonar îmbunătățit (dacă nu există reflexul Eisenmenger), cardiomegalie - ambii ventriculi și atriul drept sunt măriți, arcul arterei pulmonare se umflă.
 Orez. 11.22. Radiografia în proiecția anteroposterioră a unui pacient cu TSA primar. Modelul pulmonar este slăbit (reflexul Eisenmenger), arcul arterei pulmonare se umflă, un ventricul drept mărit și o ramură dreaptă mărită a arterei pulmonare sunt vizibile, arcul aortic este redus
Orez. 11.22. Radiografia în proiecția anteroposterioră a unui pacient cu TSA primar. Modelul pulmonar este slăbit (reflexul Eisenmenger), arcul arterei pulmonare se umflă, un ventricul drept mărit și o ramură dreaptă mărită a arterei pulmonare sunt vizibile, arcul aortic este redus
Cu ecocardiografia în poziția apicală cu patru camere în modul B, un ASD este clar vizibil (Fig. 11.23, vezi insertul). Se poate observa că defectul este situat direct deasupra valvelor atrioventriculare, adică. este primară, UIA secundară intactă de la baza inimii este clar vizibilă. Pe fig. 11.24 (vezi insertul) cu ajutorul Doppler color se demonstrează fluxul de sânge din atriul stâng spre părțile drepte ale inimii. EcoCG al unui pacient cu TSA primar în modul B în poziția parasternală a axei scurte a ventriculului stâng la nivelul valvei mitrale arată clar despicarea foiței anterioare a valvei mitrale (Fig. 11.25 A, vezi insertul) . În comparație cu ecocardiografia persoana sanatoasa vedem că în mod normal avem
există continuitate a foițelor valvei mitrale (Fig. 11.25 B, vezi insert).
Metodele de confirmare de cercetare sunt cateterizarea cavităților inimii și angiografia.
Diagnosticul diferențial se realizează cu TSA secundar și insuficiență mitrală izolată. ASD secundar se caracterizează printr-o deviație a axei electrice a inimii spre dreapta și/sau blocarea ramurii drepte a fasciculului His, și cu insuficiență mitrală izolată, dilatare semnificativă a atriului stâng, care nu apare cu ASD.
Chirurgia cardiacă este absolut indicată pentru decompensare și cu insuficiență mitrală în creștere, dacă nu există sindromul Eisenmenger.
ASD primar este o variantă a unui canal atrioventricular parțial deschis. Este adesea combinată cu despicarea valvei mitrale.
Anevrism congenital al sinusului Valsalva- aceasta este o bombare în formă de deget sau sacculară a peretelui aortic al sinusului Valsalva în lumenul camerei adiacente acestuia. Mai des există un anevrism al sinusului coronar drept, care se umflă în lumenul atriului drept sau al ventriculului drept. Un anevrism al sinusului non-coronar bombat în atriul drept. Poate exista o mică perforație la vârful anevrismului. Originea defectului este o încălcare a conexiunii stratului muscular al peretelui aortic cu inelul fibros al valvei aortice în embriogeneză și eșecul părții membranoase a septului. Pătrunderea unui anevrism în camera adiacentă a inimii (Fig. 11.26) se explică prin impactul hemodinamic constant asupra anevrismului sau o singură „lovitură” hemodinamică în timpul activității fizice ridicate, adăugarea de endocardită infecțioasă.
Înainte de ruptură, anevrismul nu modifică semnificativ hemodinamica, cu excepția cazurilor rare când creează o obstrucție a fluxului de sânge în tractul de ieșire al ventriculului drept. Când se rupe, are loc o descărcare bruscă de sânge din aortă în inima dreaptă, ceea ce duce la o creștere rapidă a fluxului sanguin pulmonar și rapid
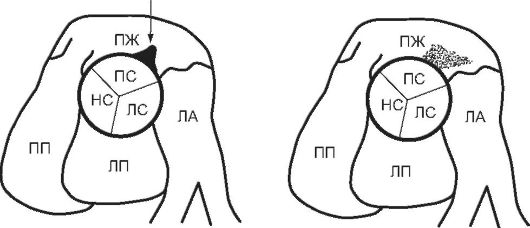 Orez. 11.26. Reprezentare schematică a unui anevrism congenital al sinusului Valsalva și ruptura acestuia în ventriculul drept. RA - atriul drept, LA - atriul stâng, RV - ventriculul drept, LA - artera pulmonară, PS - sinusul coronar drept, LS - sinusul coronar stâng, NS - sinusul necoronar
Orez. 11.26. Reprezentare schematică a unui anevrism congenital al sinusului Valsalva și ruptura acestuia în ventriculul drept. RA - atriul drept, LA - atriul stâng, RV - ventriculul drept, LA - artera pulmonară, PS - sinusul coronar drept, LS - sinusul coronar stâng, NS - sinusul necoronar
Creșterea volumului de sânge de la romi care curge în partea stângă a inimii. Supraîncărcarea progresivă a volumului părților drepte și stângi ale inimii duce la insuficiență cardiacă acută.
Ruptura unui anevrism congenital al sinusului coronar apare de obicei la 30-40 de ani, mai rar la 50-60 de ani. Se manifestă ca sever simptome clinice- dezvolta dureri in inima, tahicardie, colaps, cianoza severa. Cel mai frecvent diagnostic este infarctul miocardic. Spre deosebire de un atac de cord, împreună cu simptomele unei rupturi, apare un suflu prelungit sistole-diastolic grosier în regiunea inimii. Localizarea zgomotului depinde de locul străpungerii - atunci când un anevrism se sparge în atriul drept, zgomotul se aude în spațiul intercostal III-IV deasupra sternului sau în dreapta acestuia, cu o străpungere în ventriculul drept. - la nivelul spaţiului intercostal II-IV din spatele sternului.
Diagnosticul se bazează în primul rând pe ecocardiografie, ecocardiografia transesofagiană fiind metoda definitorie. Cu acesta, este posibil să se vizualizeze anevrismul și cu ajutorul ecocardiografiei Doppler - resetarea. În unele cazuri, când un anevrism al sinusului Valsalva se rupe, foița valvei aortice este adesea atrasă în defect de către fluxul sanguin și se dezvoltă regurgitare aortică de severitate diferită. În unele cazuri, cerceveaua trasă în defect îl închide, scurgerea sângelui din aortă în ventriculul drept se oprește și starea pacienților se îmbunătățește, dar acest lucru se întâmplă rar.
Diagnosticul unui anevrism congenital rupt al sinusului Valsalva trebuie pus de urgență, iar pacientul trebuie trimis imediat la un chirurg cardiac.
Anevrism congenital al sinusului Valsalva- aceasta este o bombare a peretelui aortic al sinusului (cel mai adesea cel drept) în lumenul camerei adiacente acestuia. Când un anevrism se rupe, are loc șuntarea sângelui de la aortă la inima dreaptă, ceea ce duce la creșterea fluxului sanguin pulmonar și a afluxului către inima stângă, provocând supraîncărcare de volum și insuficiență cardiacă acută.
alte malformații cu care pacienții supraviețuiesc până la vârsta adultă
situs inversus
situs inversus- transpunerea corectată arterele principale, bloc atrioventricular complet congenital, una dintre anomaliile de localizare a inimii în torace.
Sinonime: inima dreapta pe partea stângă, dextrocardie adevărată, dextrocardie în oglindă. Este o imagine exactă în oglindă a unei inimi normale. De obicei împreună cu situs inversus, pe lângă o anomalie în localizarea inimii în piept, există un aranjament complet invers al organelor. Dacă nu există malformații cardiace congenitale concomitente, care sunt mai frecvente în dextrocardia adevărată decât în populația generală, pacienții trăiesc până la bătrânețe, uneori neștiind nimic despre anomalia lor. situs inversus ușor de detectat prin examenul electrocardiografic. În astfel de cazuri, complexul QRS în plumb din mana dreapta(aVR) arată ca în plumb din mâna stângă (aVL) și invers - în aVL arată ca în aVR; în derivația standard II, ca și în derivația III și invers. La plumbul standard I, dinții au direcția opusă față de cea normală. AVF plumb nu este modificat. Acestea. electrocardiograma arată ca și cum electrodul din mâna dreaptă este suprapus în stânga, din stânga - în dreapta. În derivațiile toracice, amplitudinea complexului QRS scade spre derivațiile stângi. Dacă schimbați electrozii de pe mâini pe alocuri și puneți electrozii toracici într-o oglindă în raport cu locația lor obișnuită, electrocardiograma va căpăta un aspect normal.
O examinare cu raze X determină, de asemenea, cu ușurință anomalia locației inimii în piept.
Astfel de pacienți nu necesită tratament, dar ar trebui să fie observați de un cardiolog, deoarece pot avea un curs asimptomatic de malformație congenitală.
Transpunerea corectată congenitală a marilor vase
Transpunerea marilor vase (TMS) se numește defecte în care aorta pleacă din ventriculul drept al inimii, iar trunchiul pulmonar din stânga. În TMS completă, aorta transportă sânge neoxigenat către organele circulației sistemice, în timp ce artera pulmonară transportă sânge oxigenat. Valvele atrioventriculare și ventriculii sunt formați corect. Venele goale și pulmonare sunt conectate corect la atriul drept și cel stâng. Cu TMS complet, cercurile de circulație sunt deconectate, iar viața nu este posibilă fără așa-numitele defecte compensatoare - VSD și ASD. Astfel de pacienți trăiesc rar până la vârsta adultă fără tratament.
Transpunerea corectată a marilor vase (CTMS) este un defect în care atriul drept morfologic normal prin valva atrioventriculară, care este anatomic mitrală, este conectat la ventriculul stâng normal, din care pleacă artera pulmonară. Atriul stâng morfologic normal este conectat la ventriculul drept anatomic prin valva atrioventriculară, care este anatomic tricuspidă, din care pleacă aorta. În acest caz, cercurile de circulație nu sunt separate și pentru o lungă perioadă de timp există o hemodinamică normală. În absența unei malformații congenitale concomitente, MTMS nu se manifestă clinic mult timp. La unii pacienți din copilărie sau vârsta adultă se dezvoltă blocaje atrioventriculare de gradul II-III, care se pot manifesta sub formă de amețeli, leșin etc.
La auscultare, se poate detecta un sunet II puternic la baza inimii, care este creat de valva aortică în poziția anterioară. Unii pacienți au insuficiență a uneia sau alteia valve atrioventriculare de severitate variabilă, manifestată prin zgomotul corespunzător. Raze X dezvăluie o formă sferică a umbrei inimii pe fundalul fluxului sanguin pulmonar normal. Datorită stângii
locația aortei, conturul stâng sus al umbrei cardiovasculare nu se diferențiază în prima și a doua arcade (arcade aortice și artere pulmonare).
Acest defect poate fi diagnosticat prin ecocardiografie. Totodată, se dezvăluie valva mitrală situată în față, iar valva tricuspidiană este situată în spatele, în spatele septului interventricular, contactul mitro-pulmonar în locul celui mitro-aortic. Prezența unui IVS exclude un singur ventricul.
Diagnosticul este confirmat cu cateterism cardiac. În absența blocului atrioventricular complet, tratamentul chirurgical nu este necesar la pacienții cu ATM.
malformații frecvente în care probabilitatea de a supraviețui până la maturitate este scăzută
Tetralogia lui Fallot
Acest defect se caracterizează prin patru semne: stenoza indubulară a arterei pulmonare; VSD, hipertrofie miocardică a ventriculului drept și dextropoziție aortică. Datorită VSD subaortică, aorta este „în vârf” pe doi ventricule, iar sângele intră în ea atât din ventriculul stâng, cât și din ventriculul drept. Cantitatea de sânge venos care intră în aortă din ventriculul drept depinde de raportul dintre dimensiunea VSD și severitatea stenozei tractului de ieșire al ventriculului drept. Datorită VSD-ului mare, se stabilește o presiune egală în ventriculi. În stenoza moderată a arterei pulmonare, șuntarea de la dreapta la stânga poate să nu fie prezentă, iar astfel de copii nu au cianoză (așa-numita formă palidă, acianotică a tetralogiei Fallot). În cazul stenozei severe, există de obicei un șunt încrucișat sau dreapta-stânga de sânge prin VSD. VS este subîncărcat, de dimensiuni reduse, dar la pacienții adulți valoarea sa se apropie de normal din cauza circulației colaterale emergente.
Fără tratament chirurgical, doar 1% dintre pacienți supraviețuiesc până la vârsta de 30 de ani și 10% supraviețuiesc până la vârsta de 20 de ani (N.A. Belokon, V.P. Podzolkov, 1991).
Tabloul clinic în copilărie constă în cianoză, dificultăți de respirație și toleranță scăzută la efort. Copil
in timpul repausului, genuflexiuni sau minciuni cu picioarele aduse la stomac. S-a demonstrat că această postură mărește întoarcerea sângelui din jumătatea inferioară a corpului și ajută la reducerea hipoxemiei.
Prezența hipoxemiei duce la o modificare a degetelor sub formă de „ochelari de ceas” și „tobe”. Pentru copiii cu vârsta cuprinsă între trei luni și doi ani, așa-numitele convulsii cianotice sunt caracteristice: brusc copilul devine neliniștit, dificultăți de respirație, cianoza crește, apare apnee, pierderea conștienței (comă hipoxică), convulsii, hemipareză. Apariția unor astfel de atacuri este asociată cu spasmul secțiunii indibulare a ventriculului drept, rezultând în întregime sânge dezoxigenat prin VSD intră în aortă și provoacă hipoxie cerebrală.
Pacienții cu stenoză pulmonară minoră supraviețuiesc de obicei până la vârsta adultă, astfel încât cianoza este de obicei absentă sau nu este pronunțată. Există adesea un decalaj dezvoltarea fizică. Toleranța lor la activitatea fizică este redusă, sunt posibile plângeri de durere în regiunea inimii. Dificultățile de respirație și tahicardia sunt asociate mai des nu cu insuficiența cardiacă, ci cu hipoxemie. Palparea toracelui evidențiază tremor sistolic. La unii pacienți, temperatura crește periodic, ceea ce este asociat cu o tulburare în termoreglare din cauza hipoxiei cronice prelungite a centralei. sistem nervosși este adesea confundat cu accesarea endocarditei infecțioase.
Auscultarea evidențiază un suflu de ejecție sistolic grosier în spațiul intercostal II-IV din stânga sternului, creat de stenoză pulmonară. Primul ton este întărit. Tonul II peste artera pulmonară este slăbit. Nu există zgomot VSD, pentru că presiunea în ventriculi este aceeași.
Pe ECG la pacienții cu tetradă Fallot de vârstă matură, se evidențiază o rightogramă, semne de hipertrofie miocardică a ventriculului drept, uneori blocarea ramurii drepte a fasciculului His, extrasistolă, semne de suprasolicitare a atriului drept.
Pe radiografiile toracelui în proiecția anteroposterioră, există o depleție a modelului pulmonar, prezența colateralelor, un arc înfundat al arterei pulmonare și un vârf rotunjit al ventriculului stâng (umbra inimii sub forma unei „pantof de lemn”). În poziția II oblică sunt relevate semne de hipertrofie a ventriculului drept. Umbra inimii nu este extinsă. Dacă stenoza pulmonară nu este
exprimat, apoi pe radiografie pot exista semne de VSD - o creștere a modelului pulmonar.
EchoCG în modul B relevă dextropunerea aortei, folosind ecocardiografia Doppler pentru a identifica și determina gradul de evacuare a ventriculului drept, dimensiunea trunchiului arterei pulmonare, dimensiunea ventriculului drept și severitatea hipertrofiei acestuia.
Metoda de diagnostic final este cateterismul cardiac.
Chirurgia cardiacă este indicată tuturor pacienţilor „simptomatici”, indiferent de vârstă.
Tetralogia lui Fallot se caracterizează prin patru caracteristici: stenoză pulmonară infundibulară, VSD, hipertrofie miocardică a ventriculului drept și dextropoziție aortică.
VSD nerestrictiv
Spre deosebire de VSD-urile restrictive, VSD-urile mari nerestrictive apar de obicei încă de la început copilărie timpurie, astfel de pacienți supraviețuiesc rar până la vârsta adultă. În astfel de cazuri, volumul șuntului de sânge de la stânga la dreapta este determinat de raportul de rezistență în aortă și artera pulmonară și poate fi destul de mare. Aceasta duce la o suprasolicitare semnificativă a volumului ambilor ventriculi și la dezvoltarea hipertensiunii pulmonare.
Cu toate acestea, un număr mic de pacienți cu DVS nerestrictive nu foarte mari supraviețuiesc până la vârsta adultă. De obicei, aceștia sunt pacienți cu un fizic nedezvoltat, adesea se găsește o cocoașă la inimă. Tremuratul sistolic este rar.
În timpul auscultării la vârful inimii, primul ton este intensificat, iar accentul și despicarea celui de-al doilea ton se aude pe artera pulmonară. Suflu sistolic de volum și durată variată se aude în spațiul intercostal III-IV din stânga sternului. Cu toate acestea, cu o creștere a hipertensiunii pulmonare, atunci când presiunea în ventriculul drept și stânga devine aproape, este posibil să nu existe zgomot.
Pe ECG, există de obicei semne de hipertrofie și supraîncărcare a părților stângi și drepte ale inimii, în ciuda acestui fapt, există adesea o rightogramă (Fig. 11.27).
Când radiografia în proiecția anteroposterioră evidențiază un model pulmonar îmbunătățit, dacă nu există sindrom Eisenmenger și
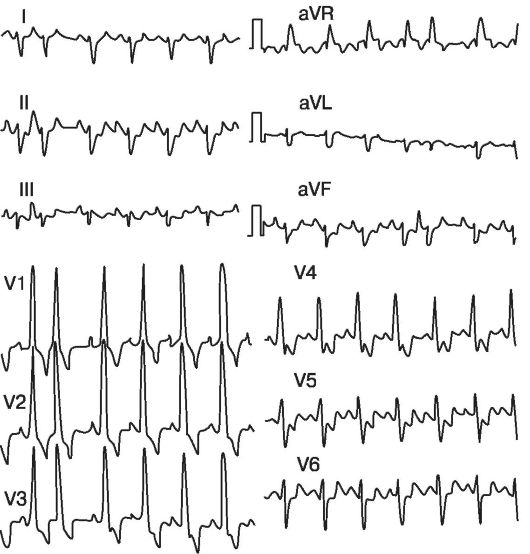 Orez. 11.27. ECG al unui pacient cu VSD non-restrictive și sindrom Eisenmenger. ECG de tip 5, val târziu de amplitudine mare R aVR, undele R ridicate V1-3 și profunde 5 y5 _ 6 indică hipertrofie severă a ventriculului drept al inimii
Orez. 11.27. ECG al unui pacient cu VSD non-restrictive și sindrom Eisenmenger. ECG de tip 5, val târziu de amplitudine mare R aVR, undele R ridicate V1-3 și profunde 5 y5 _ 6 indică hipertrofie severă a ventriculului drept al inimii
oarecare hipertensiune pulmonară, inima este mărită atât din cauza ventriculilor, cât și a atriilor, arcul arterei pulmonare se umflă de-a lungul conturului stâng (Fig. 11.28).
EchoCG în modul B (Fig. 11.29) este capabil să vizualizeze VSD și să determine dimensiunea acestuia. Folosind Doppler color (Fig. 11.30, vezi insert), se demonstrează fluxul sanguin prin defect. Cel mai bine se văd defectele perimembranoase și subarteriale, defectele din partea sa musculară sunt mai grave.
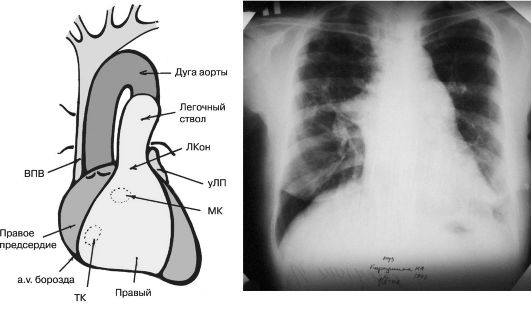
Orez. 11.28. Radiografia în poziția anteroposterioră a unui pacient cu VSD nerestrictive și sindrom Eisenmenger. Modelul pulmonar este slăbit, arcul arterei pulmonare se umflă
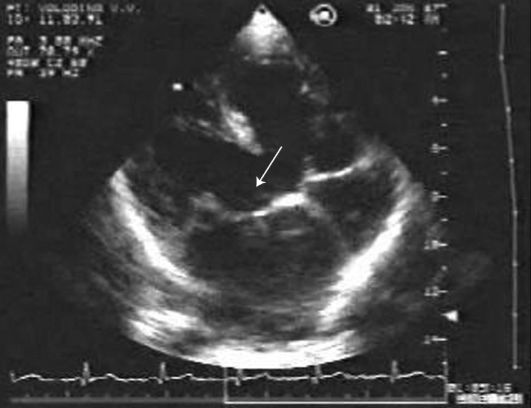 Orez. 11.29. Ecocardiografia în modul B a unui pacient cu defect septal ventricular nerestrictor, poziție apicală cu patru camere. Fluxul subarterial VSD este clar vizibil
Orez. 11.29. Ecocardiografia în modul B a unui pacient cu defect septal ventricular nerestrictor, poziție apicală cu patru camere. Fluxul subarterial VSD este clar vizibil
Cu un VSD non-restrictiv diagnosticat pentru prima dată la un pacient adult, examinarea suplimentară și tacticile de tratament sunt discutate cu un chirurg cardiac. În fiecare caz, se ia o decizie privind necesitatea cateterizării și posibilitatea intervenției chirurgicale.
ÎN În ultima vreme S-a realizat o îmbunătățire semnificativă a metodelor de diagnostic și tratament al malformațiilor cardiace congenitale. Datorită progreselor în diagnostic și tratament, copiii cu malformații cardiace congenitale sunt capabili să trăiască in varsta. Mai mult, este de așteptat să crească numărul pacienților cu boli cardiace congenitale tratați în copilărie și ajungând la vârsta adultă. Potrivit estimărilor preliminare, aproximativ 200.000 de adulți din țara noastră suferă de malformații cardiace congenitale.
Malformațiile cardiace congenitale la adulți pot fi împărțite în general în două grupuri. Primul grup include cei a căror boală nu a fost recunoscută și care au fost diagnosticați recent (cele mai frecvente boli sunt TSA și valva aortică bicuspidă); celălalt grup este format din cei care au fost observați și primiți tratament medicamentos din copilărie. Un anumit număr de pacienți din al doilea grup pot suferi de o boală gravă și pot suferi una sau mai multe operații, în timp ce pacienții din celălalt grup pot să nu aibă boala grava necesită intervenție chirurgicală.
Pentru grup Risc ridicat includ pacienții care au suferit una sau mai multe operații, precum și pacienții cu boli cardiace congenitale, însoțite de cianoză, contracții anormale ale inimii și presiune ridicataîn artera pulmonară. La astfel de pacienți, în timp, pot apărea și alte probleme care prezintă probabilitatea unui risc pentru viață. Unele probleme care sunt ușor de depășit în copilărie devin grave la vârsta adultă. În timp ce intervențiile terapeutice acordate unor pacienți în timpul copilăriei sunt în întregime remediative, singurul scop pentru alți pacienți este de a se asigura că ajung la maturitate în siguranță. Acești pacienți vor fi supuși unor intervenții chirurgicale suplimentare, angiografie, spitalizare și urmărire în secția de terapie intensivă când vor ajunge la vârsta adultă.
Îngrijirea ulterioară și tratamentul pacienților adulți cu boli cardiace congenitale necesită cunoștințe și abilități specifice. O clinică este necesară pentru a oferi servicii acestor pacienți. perioadă de tranziție. Cardiologii care lucrează cu pacienți adulți nu au suficientă experiență pentru a rezolva complexul și probleme serioase pacienți adulți cu boală cardiacă congenitală. Cardiologii pediatri nu se ocupă de problemele de sănătate ale adulților. Din acest motiv, cardiologii pediatri și cardiologii adulți trebuie să lucreze în comun.
Adulții cu boli cardiace congenitale ar trebui să fie informați în detaliu despre sarcină, alegerea carierei, volumul de exerciții fizice și stilul de viață. Număr mare pacientele pot avea un copil numai sub supraveghere. Pentru astfel de pacienți, este necesară o consultare cu un genetician înainte de a lua o decizie de a avea un copil. Trebuie făcută o evaluare a riscului pentru pacient; acei pacienti care prezinta un risc crescut ar trebui sa fie informati despre contraceptive, iar sarcina este intrerupta daca circumstantele o impun.
Boala cardiacă congenitală la copii și adulți
Încălcarea formării structurii inimii cu Dezvoltarea embrionară numită boală cardiacă congenitală. Boala cardiacă congenitală la copii este de obicei detectată încă din primele zile de viață, dar există cazuri când pacientul detectează o modificare a structurii inimii deja la vârsta adultă.
Un defect în structura inimii și a arterelor sale duce la afectarea fluxului sanguin în organul însuși. Și întrucât inima este organul principal care pompează sânge pentru întregul corp, bolile de inimă sunt pline de consecințe grave pentru întregul corp, inclusiv moartea. Uneori, în cazuri severe.
Pentru mulți părinți, din cauza necunoașterii caracteristicilor medicale ale bolii, un astfel de diagnostic sună ca o propoziție. Iar la adulți, când diagnosticul este confirmat, starea de spirit este departe de a fi optimistă. Dar Medicină modernă atât de reușit în tratamentul unor astfel de boli încât majoritatea pacienților după operație duc o viață lungă și fericită.
Boli cardiace congenitale: cauze
Până în prezent, există două cauze globale principale care afectează dezvoltarea această boală– influență externă și genetică. LA influente externe includ motive de mediu.
Cu o combinație negativă a ambilor factori, probabilitatea de a avea un copil cu diagnostic de boală cardiacă congenitală este extrem de mare. Astăzi, statisticile pentru nou-născuți sunt necruțătoare - fiecare sută de copil se naște cu un diagnostic similar.
Boli cardiace congenitale: cauze care cresc riscul bolii:
- predispoziție genetică - prezența unei boli la unul dintre părinți;
- boli infecțioase transferate în timpul sarcinii - citomegalovirus, rubeolă, gripă, virus herpes simplex etc.;
- boli psihosomatice viitoare mamă, inclusiv diabet zaharat;
- obiceiuri proaste - fumat, alcoolism, droguri;
- ecologie nocivă - a fi într-un mediu nociv pentru o perioadă lungă de timp (producție, întreprinderi chimice etc.).
Boala cardiacă congenitală la adulți
Boala cardiacă congenitală la adulți nu apare după anumită perioadă. De aceea este înnăscut. Doar că gradul defectului în structura inimii poate fi atât de ușor încât nu a putut fi diagnosticat la naștere. Și primele semne au început să apară abia mulți ani mai târziu. De obicei, modificările structurii inimii la adulți sunt detectate după alte boli ale inimii - ateroscleroza. atacuri de cord etc. Cu aceste afecțiuni, sunt prescrise o ecografie a inimii și un ECG. Și în cursul studiului, este dezvăluită boala cardiacă congenitală la adulți.
Oamenii de știință văd motivele dezvoltării bolilor de inimă asociate cu sexul. O serie de studii au arătat că femeile suferă de această boală de multe ori mai des decât bărbații. Cu toate acestea, în funcție de tipul de boală cardiacă, acestea pot fi împărțite condiționat în „feminin”, „masculin” sau „neutru”.
Adică, tipurile feminine includ astfel de tipuri de boli precum:
- canal arterios deschis;
- defect septal atrial;
- defect de sept ventricular;
- „Ansamblu” de defecte în îngustarea gurii arterei pulmonare, septului atrial și hipertrofia ventriculului drept.
Tipul „masculin” de dezvoltare anormală a inimii includ:
- stenoză aortică congenitală;
- transpunerea marilor vase;
- coarctația aortei;
- conexiune anormală a venelor pulmonare.
Următoarele defecte pot fi atribuite tipului „neutru” al bolii, adică aceleași care apar la ambele sexe:
- încălcarea structurii septului aorto-pulmonar;
- stenoza arterei pulmonare;
- defect septal atrial tip 1;
- anomalie Ebstein;
- atrezia valvei tricuspidiane.
Când vorbim despre statistici în „favoarea” femelei, înseamnă că anomaliile de dezvoltare de tip „feminin” sunt mult mai frecvente la adulți și copii decât anomaliile în structura inimii celorlalte două tipuri.
Cauze și tipuri de malformații cardiace congenitale
Majoritatea nou-născuților sunt diagnosticați în prima lună de viață. Acest lucru se datorează îmbunătățirii sistemului de examinare a copiilor. Boala cardiacă congenitală la copii poate fi detectată numai cu ajutorul unei ecografii a inimii. Motivele, de fapt, sunt aceleași ca și în cazul bolilor de inimă la adulți - genetică și factori externi.
Din păcate, statisticile mortalității pentru bolile cardiace congenitale la copii sunt îngrozitoare. Până la un an, 87% dintre copii mor în cursul natural al bolii. Pentru a lupta pentru reducerea acestor numere, medicii au dezvoltat propria clasificare a CHD pentru a identifica cursul bolii și tratamentul acesteia.
- Hipoplazie. Conduce la subdezvoltarea ventriculului stâng sau drept. Adică, cu un astfel de sindrom, doar o parte a inimii funcționează la capacitate maximă. Din fericire, hipoplazia este rară la copii. Aceasta este una dintre cele mai periculoase forme de încălcare a structurii inimii.
- defect de obstrucție. Se caracterizează prin atrezie sau stenoză a venelor, valvelor cardiace sau arterelor.
- Modificarea structurii partiției. Atriul stâng și cel drept sunt separate printr-un sept. Acest tip de boală cardiacă se caracterizează printr-o scădere a eficienței de pompare a sângelui datorită faptului că, din cauza unui defect de perete, sângele se deplasează din partea stângă a inimii în partea dreaptă.
- Viciu albastru. Și-a primit numele datorită dobândirii unui ton al pielii gri-albăstrui din cauza lipsei de oxigen din sânge. Defectul albastru duce la cianoză.
Dacă boala cardiacă este detectată la copii, cel mai adesea prescris intervenție chirurgicală. Terapia acționează mai degrabă ca o funcție auxiliară pentru a scăpa de boală.
Prevenirea bolilor de inima
Până în prezent, din păcate, nu există așa ceva profilactic, ceea ce te-ar scuti 100% de posibilitatea de a dezvolta boli de inima. Cu toate acestea, există persoane expuse riscului și pot fi luate anumite măsuri pentru aceștia. Aceștia sunt pacienți care au fost atacați de streptococ. Cea mai frecventă cauză a anginei este, printre altele, bacilul streptococic. Pe baza deteriorării corpului cu acest stick, se dezvoltă reumatismul, care poate duce la dezvoltarea bolilor de inimă.
Malformații cardiace congenitale la adulți
Defect septal atrial (ASD)
Boala este de obicei asimptomatică până în a treia sau a patra decadă de viață, când se dezvoltă dispnee la efort, oboseală și palpitații.
Simptomele de mai sus sunt adesea însoțite de hipertensiune pulmonară (vezi mai jos).
Examinare fizică
Bătăi ventriculare drepte parasternale, zgomot cardiac larg, fix, divizat II, suflu sistolic de-a lungul marginii sternului, suflu diastolic, „zgomot” al fluxului sanguin prin valva tricuspidă, o undă proeminentă v pe flebograma jugulară.
Blocarea incompletă a piciorului drept al mănunchiului lui His. Deviația axei spre stânga este adesea observată cu un defect septal inferior.
Radiografia toracelui
Întărirea modelului vascular pulmonar, ventriculul drept proeminent și trunchiul arterei pulmonare (atriul stâng nu este de obicei mărit).
ZhoKG
Dilatarea atriului drept și a ventriculului drept; pe ecocardiografia Doppler - o încălcare a turbulenței fluxului transatrial.
Angiografia cu radionuclizi
Evaluarea neinvazivă a raportului dintre fluxul sanguin pulmonar / fluxul sanguin sistemic (LC / SC).
Tactici medicale
Dispneea și palpitațiile pot fi controlate cu digitalice și diuretice ușoare (hidroclorotiazidă 50 mg pe zi). Într-un TSA cu un raport al fluxului sanguin pulmonar și sistemic > 1,5:1,0, se recomandă chirurgia reconstructivă. Intervenția chirurgicală este contraindicată la pacienții cu hipertensiune pulmonară semnificativă și un raport al fluxului sanguin pulmonar și sistemic de 1,5:1. Utilizarea antibioticelor este importantă pentru prevenirea endocarditei.
Ductus arteriosus patent (PDA)
Comunicarea patologică între aorta descendentă și artera pulmonară este asociată cu nașterea în munți, cu rubeola gravidă.
Anamneză
Cursul asimptomatic al bolii sau respirația scurtă și oboseala în timpul efortului sunt caracteristice.
Examinare fizică
Bătăi apex pronunțate; zgomot puternic de „mașină” la marginea stângă a sternului în secțiunea superioară. Componenta diastolică a suflului poate dispărea odată cu dezvoltarea hipertensiunii pulmonare.
Hipertrofia ventriculară stângă este frecventă; hipertrofia ventriculară dreaptă în hipertensiunea pulmonară.
Întărirea modelului vascular pulmonar, extinderea trunchiului arterei pulmonare, aorta ascendentă, ventriculul stâng, uneori calcificarea ductului.
ecocardiografie
Un ventricul stâng hiperdinamic, mărit, PDA este adesea identificat prin ecocardiografie bidimensională. Ecocardiografia Doppler permite stabilirea fluxului sanguin intracardiac patologic.
Tactici medicale
Hipertensiune pulmonară progresivă (PLH)
Pacienții cu ASD, VSD sau PDA semnificativ și necorectat pot dezvolta rapid PLH ireversibilă fără bypass. oxigenate sânge în patul arterial (sunt de la dreapta la stânga). Oboseala, amețelile ușoare și durerile în piept sunt adesea datorate ischemiei ventriculare drepte, însoțite de cianoză, degete din tobă, IR puternic, suflu de regurgitare pulmonară și semne de insuficiență ventriculară dreaptă. ECG și ecocardiografia evidențiază hipertrofie ventriculară dreaptă. Corectia chirurgicala defecte congenitale contraindicat în PLH severă și prezența unui șunt de la dreapta la stânga.
Stenoza arterei pulmonare (PSA)
Cu gradient valvular transpulmonar 50 mmHg) necesită valvuloplastie chirurgicală (sau cu balon).
Coarctația aortei
Numai coarctația zonei aortice distale de gura arterei subclaviei stângi se referă la formele de hipertensiune arterială corectate chirurgical (vezi capitolul 76). De obicei, defectul este asimptomatic, dar poate fi însoțit de cefalee, oboseală sau claudicație intermitentă.
Examinare fizică
Hipertensiunea arterială a fost observată membrele superioare, precum și o slăbire a pulsului arterei femurale și o scădere a tensiunii arteriale prin membrele inferioare. Arterele colaterale pulsatorii sunt palpabile în spațiul intercostal. Suflule sistolice (și uneori diastolice) se aud cel mai bine în partea superioară a spatelui.
ECG. Hipertrofie ventriculara stanga.
Radiografie toracică
Modele de coaste cauzate de colaterale; partea distală a arcului aortic seamănă cu numărul 3.
Tratament
Corecție chirurgicală, deși hipertensiunea arterială poate persista după intervenție chirurgicală. Chiar și după corectare, este necesară prevenirea endocarditei prin utilizarea antibioticelor.
(Harrison’s Handbook of Internal Medicine)
URO-PRO: tratamentul bolii impotenței Soci
Defectele cardiace sunt modificări patologice anormale ale valvelor unui organ, pereților acestuia, pereților despărțitori sau vaselor mari.
Ca urmare a unor astfel de modificări, circulația normală a sângelui în miocard este perturbată, ceea ce duce la dezvoltarea insuficienței și lipsa de oxigen multe organe.
Defecte în structura anatomică a regiunilor cardiace apar din mai multe motive. Acest fel patologiile duc la funcționarea necorespunzătoare a organismului și provoacă multe complicații ireversibile.
- Toate informațiile de pe site au scop informativ și NU sunt un ghid de acțiune!
- Oferiți-vă un DIAGNOSTIC EXACT numai DOCTOR!
- Vă rugăm să NU vă automedicați, dar programați o întâlnire cu un specialist!
- Sanatate tie si celor dragi!
Specii după factor etiologic
Defectele cardiace sunt împărțite în două tipuri principale în ceea ce privește mecanismul de apariție: și.
Fiecare dintre ele este împărțit în propriile grupuri, tipuri și clasificări, cu toate acestea, toate au un loc comun de localizare:
- în aparatul de supapă;
- în pereții mușchiului inimii;
- în vasele mari ale inimii.
Pericol această boală că oricare modificare patologicăîn inimă duce la circulație slabă. Este cauzată de o încetinire a fluxului sanguin și de stagnarea acestuia sistem vascular. Toate acestea provoacă multe boli asociate cu hipoxie și deficiențe nutriționale.
Ambele tipuri de defecte cardiace apar din aproape aceleași motive. Dar dezvoltarea lor are loc în momente complet diferite.
| Congenital |
|
| Dobândit | Astfel de defecte pot apărea la orice vârstă. Clasificarea defectelor cardiace dobândite este subdivizată în funcție de cauzele bolii, care pot fi leziuni de organ sau grave. boli infecțioase, a cărui complicație este reumatismul și anume:
Printre altele, defectele dobândite se dezvoltă adesea ca urmare a leziunilor pereților inimii, boala coronariană, hipertensiune arterială cronică etc. |
Tipuri de defecte în structura anatomică a structurilor inimii
Pe lângă mecanismul de apariție, defectele cardiace sunt de obicei împărțite în tipuri în funcție de localizarea defectului, complexitatea lor și caracteristicile consecințelor.
Deci, anomaliile cardiace în rândul medicilor sunt împărțite în următoarele tipuri:
În funcție de localizarea defectelor, boala se distinge prin următoarea clasificare:
- defecte ale supapei;
- defecte ale septului interventricular;
Care, la rândul lor, se împart în:
De asemenea, pentru defecte în structura anatomică bolile de inimă se disting prin astfel de boli:
În plus, toate aceste tipuri și tipuri se disting prin combinațiile lor atunci când pacientul are două sau mai multe modificări anatomice enumerate mai sus.
Diviziunea în funcție de hemodinamică
Pe baza hemodinamicii, defectele cardiace sunt împărțite în patru grade, care diferă în modificările existente și dezvoltarea lor:
- modificări minore;
- moderat manifestat;
- schimbări bruște;
- Terminal.
Toate aceste grade se caracterizează prin prezența unor semne care apar atunci când există o lipsă de oxigen într-un anumit loc din organism.
Pe baza caracteristicilor consecințelor, anomaliile cardiace de acest fel sunt grupate în următoarele tipuri:
Defectele albe în funcție de gradul de dezvoltare și localizarea hipoxiei sunt împărțite în patru tipuri:
Defectele albastre, spre deosebire de cele albe, au doar două tipuri, caracterizate prin îmbogățirea sau epuizarea circulației (mice) pulmonare.
În plus, defectele cardiace sunt împărțite în patru grade, determinate pe baza tulburărilor circulatorii.
Fiecare dintre ele se caracterizează prin agravarea simptomelor, prezența complicațiilor și severitatea tratamentului:
- ușoară deteriorare a circulației sângelui;
- schimbare moderată;
- fluxul sanguin afectat semnificativ;
- afectarea terminală a fluxului sanguin.

Combinate
Defecte cardiace combinate sunt destul de frecvente. Tabloul lor clinic și anatomic este alcătuit dintr-un set de semne pe care fiecare defect le are separat. Dar, în același timp, unele simptome încă se schimbă, ceea ce se manifestă prin slăbirea sau agravarea lor.
Defectele combinate sunt clasificate în:
|
|
| Triada lui Fallot | Patologia este determinată de stenoza din partea laterală a trunchiului pulmonar, o modificare a septului care separă ventriculii și hipertrofia ventriculului drept. |
| O boală care are un defect la nivelul septului atrial, combinat cu patologii de tetralogie Fallot. | |
| Malformații congenitale caracterizate prin prezența insuficienței cardiace de la valva tricuspidă și. |
Pentru a determina anomaliile combinate, este necesar să se utilizeze mai multe metode de diagnostic instrumental. Cel mai adesea, acest lucru se face folosind o radiografie toracică, electrocardiogramă, ecocardiografie și cateterism cardiac.

Cu defecte ale septului interventricular și coartării aortei, se vor observa următoarele semne:
- dispnee;
- durere de cap;
- oboseala fara cauza;
- umflarea venelor de la gât;
- pulsația și mărirea ficatului;
- slăbiciune la nivelul picioarelor;
- sângerări nazale;
- angină pectorală.
Tetralogia Fallot și arterială deschisă se manifestă prin umflarea venelor de la extremități, eritrocitoză, tumefiere, dificultăți de respirație și bătăi rapide ale inimii. În plus, defectele combinate au zgomote străine în piept, tuse, sensibilitate a inimii și cianoză în simptome. piele.
Clasificarea defectelor cardiace în funcție de localizarea defectelor
Indiferent de etiologia, tipurile și tipurile de defecte cardiace, acestea sunt de obicei împărțite în funcție de localizarea defectelor:
- în valva mitrală;
- în valva aortică;
- în tricuspidian;
- pulmonar;
- în gaura ovală.
Fiecare locație a patologiei este responsabilă pentru o anumită eșec în funcționarea sistemelor vascular și cardiac și are, de asemenea, propria sa manifestare clinică si complicatii.
Astfel de defecte sunt împărțite în modificări anatomice. Printre care se remarcă stenoza, insuficiența, hipoplazia și atrezia. Toate au un efect direct asupra circulației sângelui și cauzează prejudiciu ireparabil sănătate.
Luați în considerare defectele cardiace prin localizarea anomaliilor mai detaliat:
| valva mitrala | Valva mitrală este situată între ventriculul stâng și atriu. Este format din mai multe părți, fiecare dintre acestea putând suferi modificări anatomice, și anume:
Fiecare dintre aceste defecte provoacă stenoza valvei mitrale, care se manifestă printr-o îngustare a lumenului între departamentele în apropierea cărora se află. Cu acest defect, foile supapei se îngroașă și cresc împreună, ceea ce reduce aria deschiderii normale la 1,5-2 cm. Cel mai adesea, cauzele sunt boli infecțioase transferate și unele anomalii congenitale ale inimii. |
| valvă aortică |
|
| Valvei tricuspide |
|
| Valvă pulmonară |
|
| gaura ovala |
|
Malformațiile congenitale sunt numite diferite anomalii ale structurii inimii sau cele mai mari vase formate în stadiul dezvoltării intrauterine. Astfel de patologii sunt comune - la aproximativ 1% dintre bebeluși.
Trebuie remarcat faptul că nu toate încălcările pun viața în pericol, multe în cele din urmă dispar de la sine. Dar diagnosticul atent și tratamentul adecvat sunt foarte importante, deoarece multe defecte fără corectarea chirurgicală în timp util pot duce la moartea pacientului.
Unele boli cardiace congenitale sunt mai frecvente la băieți sau fete și, pe această bază, sunt împărțite în trei grupuri:
- Defectele „masculin” includ transpunerea vasculară, îngustarea segmentară a aortei sau cauzate de fuziunea pereților etc.;
- CHD „feminin” includ defecte ale septurilor dintre atrii, triada lui Fallot, deschiderea ductului arterial etc.;
- Defectele neutre sau comune pentru ambele sexe includ defecte septale - atrioventriculare, aorto-pulmonare și unele alte tulburări.
Cauzele malformațiilor congenitale
UPU apartine boli ereditare, dar severitatea manifestărilor lor poate fi afectată de extern factori adversi. Acestea includ:
- Expunerea la toxic substanțe chimice din mediu inconjurator;
- Influența radiațiilor ionizante;
- Efecte secundare medicamente;
- Vârsta matură parinti, mama peste 35 de ani, tata - peste 45 de ani;
- Alcoolismul parental;
- niste boli virale purtat de mamă în timpul sarcinii.
În plus, cauzele formării CHD includ adesea toxicoza severă a femeilor însărcinate. Dar medicina modernă nu încurajează un astfel de diagnostic. Și greața severă și deteriorarea bunăstării, cel mai probabil, nu sunt cauza, ci consecința unei încălcări în dezvoltarea embrionului.
Foarte des, malformațiile sistemului cardiovascular fac parte dintr-un set mai complex de tulburări provocate de anomalie cromozomiala. Prin urmare, în orice caz, este necesară o examinare amănunțită și cuprinzătoare. Adesea, nu numai copilul, ci și părinții lui trebuie să fie examinați.
Există multe clasificări diferite ale acestei patologii. Una dintre cele mai frecvent utilizate este Nomenclatura Internațională UPU, conform căreia toate defectele sunt împărțite în trei grupe:
- Subdezvoltarea (hipoplazia) a unuia și a ventriculilor inimii. Aceasta este o tulburare rară și foarte periculoasă, majoritatea copiilor cu acest diagnostic nu trăiesc să vadă operația.
- defecte de obstrucție. Aceasta se îngustează până la închiderea valvelor și a vaselor de sânge.
- Defecte ale partițiilor (interatrial și interventricular).
- „Vicii albastre”. Acestea includ tetrada Fallot, stenoza valvei tricuspide și alte tulburări care provoacă cianoza pielii.
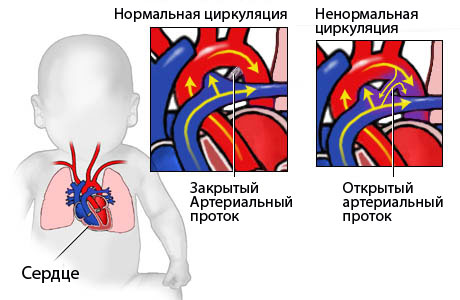
De asemenea, este adesea folosit pentru a împărți toate viciile în astfel de grupuri:
- "Palidă" nu provoacă cianoză;
- „Albastru” cu o culoare caracteristică a pielii;
- Cu ejecție încrucișată de sânge;
- Cu o încălcare a fluxului sanguin;
- Defecte ale valvei cardiace;
- defecte arteriale;
- Încălcări în secțiunile musculare ale ventriculilor (cardiomiopatie);
- Tulburări ale ritmului cardiac nu sunt asociate cu defecte ale structurii organului și ale vaselor mari care îl înconjoară.
Tabloul clinic în PWS depinde de caracteristicile defectului în sine, dar cel mai mult semne frecvente considera:
- Tentă prea palida sau albăstruie a pielii și buzelor;
- Pielea albastră când plângeți sau în timpul hrănirii;
- Scăderea temperaturii extremităților;
- Suflu în inimă (nu cu toate defectele);
- Simptomele insuficienței cardiace.
Malformațiile congenitale pot fi observate la examenele radiografice și ecocardiografice. Există și modificări ale electrocardiogramei. Uneori defectele nu se manifestă în niciun fel, iar copilul arată destul de sănătos până la aproximativ 10 ani. Apoi are respirație scurtă în timpul efortului fizic, se observă albire sau albăstruire a pielii și începe o întârziere în dezvoltarea fizică. Într-o astfel de situație, ar trebui să consultați imediat un medic.
Diagnosticarea malformațiilor cardiace congenitale
În primul rând, medicii acordă atenție semnelor descrise mai sus. De asemenea, ei iau în considerare factori precum:
- Prezența tahipneei cu retragerea coastelor;
- Prezența cianozei și răspunsul organismului la terapia cu oxigen;
- Caracteristici ale tensiunii arteriale la extremitățile superioare și inferioare;
- Natura pulsului;
- Prezența sau absența suflulor inimii;
- Cardio- și hepato-megalie.
Pentru a face un diagnostic precis, se utilizează un test de sânge, cardiografie FKG, ECG și ECHO, precum și angiografia și sondarea cardiacă.
Adesea, murmurele cardiace sunt găsite la copii fără suspiciune de boli cardiace congenitale. Cele mai multe dintre ele nu sunt periculoase, dar dacă există suflu diastolic, va fi necesar un examen cardiac suplimentar.
Defectele cardiace congenitale sunt mai susceptibile de a fi tratate metode chirurgicale. Se folosesc și cele terapeutice, dar de obicei ca auxiliare. Sunt folosite atunci când este posibil să transferați operația la mai multe întâlniri târzii pentru a lăsa copilul să crească și să devină mai puternic. Sunt utile și pentru malformațiile minore, dacă există șanse mari ca copilul să „depășească” în timp.
Foarte des, defecte cardiace congenitale sunt detectate chiar și în timpul dezvoltării fetale. În acest caz, nașterea se recomandă să fie efectuată în maternități speciale din spitalele de chirurgie cardiacă, unde este posibil să se asigure imediat avea nevoie de ajutor bebelus.
Deoarece majoritatea copiilor cu boli cardiace congenitale necesită tratament chirurgical, este important să se determine corect severitatea defectului și momentul optim pentru a efectua operația. De obicei, toate UPU-urile sunt împărțite în mai multe grupuri:
- Zero. Defectul cauzează tulburări circulatorii foarte minore și nu este necesară intervenția chirurgicală.
- Primul. Tratamentul operator poate fi efectuat într-o manieră planificată pentru un an sau mai mult.
- Al doilea. Se recomandă intervenția chirurgicală în decurs de 3-6 luni.
- Al treilea. Operația ar trebui efectuată în următoarele săptămâni.
- Al patrulea. Defectele sunt atât de grave încât este necesar un tratament chirurgical imediat în 1-2 zile.
În unele situații sunt necesare mai multe operații pentru a pune în ordine sistemul cardiovascular.
Ca adjuvant al intervenției chirurgicale, medicamentele sunt de obicei prescrise. Cel mai adesea, se recomandă să luați medicamente care îmbunătățesc metabolismul la nivelul miocardului, de exemplu, asparkam și panangin. De asemenea, sunt necesare medicamente pentru îmbunătățirea microcirculației sanguine, pentru aritmie, pentru normalizarea tensiunii arteriale și a glicozidelor cardiace.
Prognoza
Prognosticul în această situație depinde în întregime de severitatea defectului congenital și de prezența tulburărilor concomitente. De exemplu, când tulburări genetice complicat de defecte cardiace, prognosticul este extrem de nefavorabil.
Dacă CHD este singura patologie, atunci este necesar să se țină cont de caracteristicile sale și, desigur, de momentul detectării defectului. Dacă problema este identificată în timp util și tratament chirurgical poate prognosticul este favorabil. Dacă nu există oportunități de tratament complet, prognosticul este îndoielnic.
Potrivit statisticilor, malformațiile cardiace congenitale ocupă primul loc în structura mortalității nou-născuților. Dacă nu se asigură intervenția chirurgicală cardiacă calificată în timp util, aproximativ 50-75% dintre copii mor în primul an de viață. În 2-3 ani începe o perioadă de compensare, moment în care rata mortalității scade la 5%. Detectarea precoce a patologiei și corectarea chirurgicală în timp util ajută la îmbunătățirea prognosticului.
Prevenirea
Deoarece cauzele formării CHD nu sunt pe deplin înțelese, nu există metode care să le poată preveni complet. Pentru a reduce probabilitatea de a dezvolta defecte, trebuie să:
- Planificați cu atenție sarcina și evitați expunerea Substanțe dăunătoare;
- Luați medicamentele strict așa cum este prescris de medic;
- Obțineți toate vaccinurile necesare în avans și evitați contactul cu persoanele bolnave.
- Duceți un stil de viață sănătos.
Femeile peste 35 de ani au nevoie de consiliere genetică medicală și de o amănunțită diagnosticul prenatal. Chiar mai mult mare atentie din partea medicilor va fi necesar pentru viitoarele mamici cu boli cardiace congenitale. Întreaga lor sarcină trebuie observată de un ginecolog și un cardiolog. Detectarea la timp a unui defect vă va permite să atribuiți cele mai multe operațiuni întâlniri timpuriiși salvează viața copilului.
defecte congenitale inimi la copii - grup stări patologice sistemul cardiovascular, care a apărut în perioada perinatală. În funcție de tipul bolii, există o simptomatologie caracteristică, care este însoțită de o varietate de complicații. CHD la copii trebuie monitorizată și tratată în timp util, pentru a oferi copilului șansa de a trăi fără restricții.
Mecanismul de dezvoltare
Pentru dezvoltare deplină fătul are nevoie de propria circulație a sângelui, astfel încât sistemul cardiovascular se dezvoltă mai devreme decât alții - formarea începe deja în a 14-a zi după concepție. După 22 de zile, inima începe să pulseze, iar după încă câteva zile, sângele începe să circule. Și, deși sistemul cardiac în această perioadă este încă doar stadiul inițial formarea, depinde mult de modul în care procesele de dezvoltare fetală, starea mamei și factorii externi.
Malformațiile congenitale ale sistemului cardiovascular se dezvoltă între 14 și 60 de zile de la concepție. La curs normal sarcina si dezvoltare adecvată făt, până în a doua lună, inima copilului ar trebui să fie formată:
- pereții despărțitori cresc, inima devine cu patru camere;
- există o diviziune a trunchiului arterial în aortă și artera pulmonară;
- ventriculul este împărțit în două jumătăți;
- se formează valvele cardiace.
Dar influența factori negativi duce la faptul că în dezvoltarea sistemului cardiac există o insuficiență - așa se formează malformațiile congenitale.
Din a 12-a săptămână de sarcină, puteți determina ce patologii se pot dezvolta la un copil. Acest lucru le permite părinților să decidă dacă întrerupe sau continuă sarcina. Dar, trebuie avut în vedere că există posibilitatea unei erori medicale și copilul se poate naște sănătos. În orice caz, suspiciunea de boală cardiacă congenitală la un copil vă permite să vă pregătiți operațiuni posibile, care trebuie efectuat imediat după naștere pentru a-i salva viața.
Factorii care afectează dezvoltarea CHD
În cele mai multe cazuri, bolile cardiace congenitale la copii rezultă din predispozitie genetica. Dacă cineva din familie a fost diagnosticat cu boli congenitale ale sistemului cardiac, atunci cu o mare probabilitate vor fi transmise copilului.
Prezența defectelor la părinți și probabilitatea dezvoltării acestora la un copil este considerată ca procent. Astfel, stenoza aortică apare la 13% dintre cupluri dacă unul dintre părinți are antecedente de CHD. Alte tipuri de patologii apar cu o probabilitate de 1-10%.

Dezvoltarea bolilor cardiace congenitale la un copil este influențată de stilul de viață al mamei în timpul planificării sarcinii și a gestației. Aceasta include nu numai nicotina și bauturi alcoolice, dar și recepție medicamente. Ce medicamente sunt nesigure:
- diluanți de sânge cu substanta activa warfarină de sodiu (Warfarin, Marevan, Warfarex);
- anticonvulsivante și medicamente antiepileptice;
- agenți corticosteroizi;
- agenți imunosupresori;
- psihostimulante;
- barbiturice.

Risc ridicat de dezvoltare patologii congenitale inimile și alte organe la copiii ale căror mame au lucrat Condiții nefavorabile. Ridicarea greutăților sau inhalarea vaporilor chimici afectează negativ dezvoltarea fătului. Bolile infecțioase transmise de mamă sunt foarte periculoase pentru sistemul cardiac al copilului.
Chiar și o boală ușoară în primul trimestru poate afecta dezvoltarea inimii și a sistemului circulator.
Transferat în timpul sarcinii de către mamă boli infecțioase precum toxoplasmoza, rujeola, herpesul, rubeola și varicela afectează dezvoltare generală făt, inclusiv sistemul circulator.
Un rol important în formarea defectelor îl joacă bolile cronice ale mamei:
- Diabet;
- boală autoimună;
- epilepsie;
- fenilcetonurie;
- hipertensiune nefrogenă;
- patologie renală severă.

Un risc ridicat de boli cardiace congenitale la un copil, dacă mama este mai mică de 17 ani sau mai mare de 40 de ani, femeile de această vârstă ar trebui să viziteze mai des medicul și să se supună examinărilor decât altele. Dezvoltarea anormală a sistemului cardiac poate apărea când toxicoza severa primul trimestru, stres prelungit și amenințarea avortului spontan în stadiile incipiente.
Tipuri de UPU
Sunt cunoscute mai mult de o sută de CHD, iar pentru a descrie cu exactitate starea sistemului cardiac, aceste patologii sunt de obicei împărțite în funcție de mai multe criterii. În primul rând, defectele sunt determinate de locul de localizare:
- în aparatul de supapă;
- în vasele inimii;
- în pereții mușchiului inimii;
- în septul interventricular.
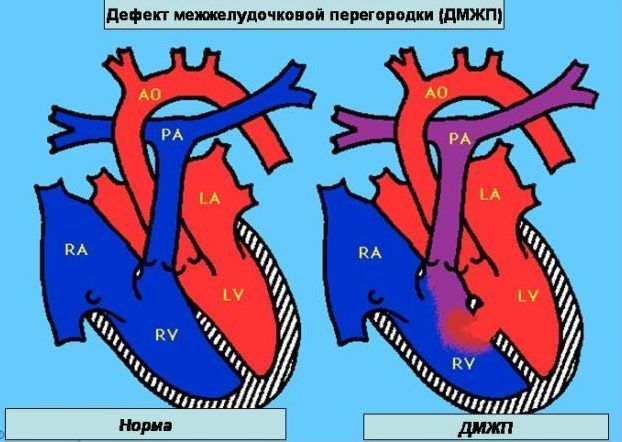
Oamenii de știință au propus mai multe clasificări ale bolilor cardiace congenitale pe motive similare, dar cea mai generală sistematizare este în „albastru” – cu prezența cianozei și „alb” – fără cianoză a pielii. Defecte "albastre" sunt diagnosticate atunci când sângele venos, intră în cerc mare circulația sângelui, pătrunde în toate țesuturile corpului, provoacă o lipsă de oxigen, ceea ce duce la cianoză.
Există două subspecii: cu îmbogățirea și epuizarea circulației pulmonare. Viciile albastre includ:
- transpunerea marilor vase;
- vase duble ale ventriculului drept;
- drenaj anormal al venelor pulmonare;
- boala Fallot;
- defectul lui Ebstein;
- trunchiul arterial comun.
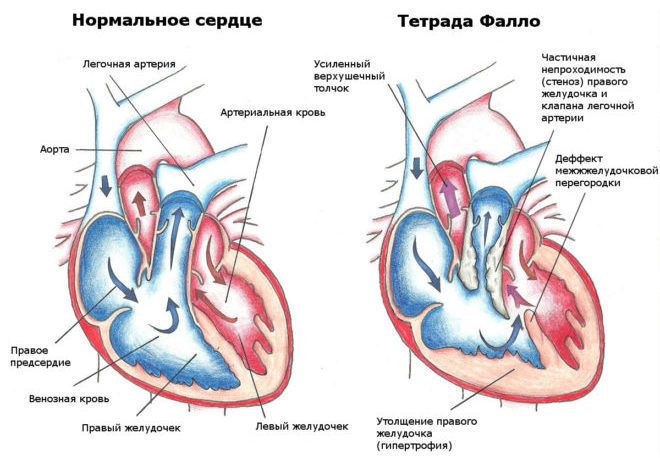
Defectele „albe” se caracterizează prin eliberarea sângelui arterial în venă. Majoritatea copiilor par complet sănătoși de mulți ani, simptomele aparând doar în timpul perioadelor crestere activa, pubertate și stres prelungit.
Anomaliile fără cianoză sunt împărțite în 4 subspecii:
- cu îmbogățirea circulației pulmonare;
- cu epuizarea cercului mic;
- cu epuizarea cercului mare;
- defecte asociate cu locație greșită inima, fara tulburari circulatorii.
Viciile albe includ:
- canal arterios deschis;
- fereastră ovală deschisă;
- coarctația aortei;
- stenoza bicuspidei, valvelor și arterei pulmonare.

Există clasificare internationala UPU, care distinge nu numai anomaliile „albe” și „albastre”, ci și următoarele tipuri:
- cu ejecție încrucișată a sângelui (o combinație de defecte cianotice și non-cianotice);
- boală valvulară a inimii;
- anomalii cu hemodinamică afectată;
- defecte ale mușchilor ventriculari;
- tulburări ale ritmului cardiac;
- defecte ale arterelor coronare.
Pe baza tulburărilor circulatorii, se disting 4 grade în funcție de creșterea semnelor:
- modificări minore;
- manifestări moderate;
- brusc;
- Terminal.
Dacă apare o etapă terminală, atunci de multe ori chiar și intervenția chirurgicală este neputincioasă, prin urmare tratamentul CHD ar trebui să înceapă în timp util.
Imaginea de ansamblu a UPU
Simptomele CHD în copilărie se pot manifesta în moduri diferite, în funcție de tipul de patologie. La unii copii, din prima zi de viata, sesizabil caracteristici boli de inimă, în altele simptomele CHD apar la cei mai tineri vârsta preșcolară, în a treia - primele manifestări anomalii congenitale dezvolta doar pentru a adolescent iar de cele mai multe ori acestea sunt vicii „albe”.
Exista simptome generale defecte cardiace congenitale:
- decolorarea pielii și a mucoaselor - fie devin albăstrui, fie devin mult mai palide decât de obicei;
- extremități în mod constant reci;
- transpirație excesivă;
- pulsația și umflarea vaselor cervicale;
- oboseală rapidă;
- somn neliniştit;
- „vânătăi” permanente sub ochi;
- scurtarea frecventă a respirației, chiar și în repaus.

Un semn suplimentar la sugari sunt buzele și obrajii albaștri în timpul hrănirii și al plânsului. Copiii cu CHD sunt foarte nelinistiti, deseori refuza sa alapteze si dorm nelinistiti. Toate acestea le afectează dezvoltarea, în comparație cu colegii sănătoși, bebelușii cu defecte încep ulterior să stăpânească abilitățile necesare, să câștige puțin în greutate.
În condiții severe, apar atacuri de sufocare și pierderea de scurtă durată a conștienței. Dar este imposibil să se facă un diagnostic de boală cardiacă congenitală numai pe aceste motive; copiii cu boli ale sistemului nervos central au simptome similare.

Insuficiența cardiacă congestivă se observă la copiii cu CHD, care se caracterizează prin dificultăți de respirație, creșterea ritmului cardiac, edem și abundență. organe interne. Evidențiez 4 grade din această stare:
- Grad ușor, care adesea nu necesită tratament. Starea copilului este stabilă, abaterile minore sunt diagnosticate în timpul examinării.
- În această etapă, simptomele sunt mai pronunțate, se observă probleme de respirație, copilul își pierde pofta de mâncare.
- Lipsa oxigenului afectează funcționarea sistemului nervos - problemelor de dezvoltare se adaugă patologiei cardiace.
- Stadiul sever (terminal) se caracterizează prin respirație deprimată și insuficiență cardiacă acută.
Aportul insuficient de oxigen la organe și țesuturi afectează metabolismul. În corpul copilului, produsele metabolice toxice încep să se acumuleze cu reacție acidă. Apare hiperaciditate- acidoză, al cărei stadiu decompensator poate fi fatal, mai ales în copilărie.
Deschideți fereastra ovală
Dintre toate tipurile de CHD, acest tip de patologie este mult mai frecventă decât altele. În mod normal, fiecare copil din perioada perinatală are o gaură între atriul drept și cel stâng, dar după naștere crește excesiv în câteva luni. La unii copii, foramenul oval poate rămâne deschis până la vârsta de doi ani, dar dacă nu crește, ci, dimpotrivă, devine mai mic, atunci această afecțiune nu necesită tratament.
Copiii cu acest defect septal atrial trebuie să facă o ecografie a inimii la fiecare 6 luni pentru a monitoriza starea acesteia în dinamică. La majoritatea copiilor, o fereastră ovală deschisă nu se manifestă în niciun fel și mulți învață despre defectul lor abia la vârsta adultă.
O fereastră ovală deschisă poate fi însoțită de următoarele simptome:
- Cianoză;
- oboseală rapidă;
- ameţeală;
- pierderea pe termen scurt a conștienței.
Copiii cu un astfel de defect sunt predispuși la răceli, așa că trebuie protejați, deoarece în timpul bolii sarcina asupra inimii și a vaselor de sânge crește.
Boala arterială deschisă
Ductusul arteriosus se află între aortă și artera pulmonară și este necesar doar în timpul sarcinii pentru transportul sângelui. Dacă nașterea a avut loc în data scadenței fara complicatii si copilul s-a nascut cu greutate normală, atunci această conductă se închide în câteva zile. La bebelușii prematuri perioada de închidere a ductului arterial poate fi de până la trei luni. Dacă după acest timp nu a existat nicio închidere, atunci se spune despre prezența unui defect congenital.
O conductă mică nu se manifestă în niciun fel și poate fi detectată doar cu ajutorul ultrasunetelor. Indirect, următoarele semne indică o conductă largă:
- decalaj în înălțime și greutate față de normă;
- având dificultăți de respirație;
- tahicardie;
- tegumente palide ale pielii;
- somn neliniştit;
- pofta slaba.

Toate aceste semne pot însoți și alte boli care nu au legătură cu sistemul cardiac, așa că este necesară o examinare amănunțită a copilului. Dacă tratamentul nu este efectuat în timp util, atunci apare o mică proeminență pe pieptul copilului. La ascultare se aud zgomote, dar doar un specialist cu experiență le poate asculta. Copiii cu această anomalie dezvoltă adesea insuficiență cardiacă, care poate duce la moartea copilului.
Transpunerea marilor vase este un defect grav în care aorta și artera pulmonară sunt localizate incorect - aorta pleacă din partea dreaptă a inimii, iar artera pulmonară din stânga. Cu o astfel de structură, cercurile mari și mici ale circulației sanguine nu comunică între ele și sângele venos nu este saturat cu oxigen.

De la naștere, copilul are cianoză persistentă, deși în primele zile starea este satisfăcătoare. Simptome care cresc treptat:
- apare scurtarea respirației;
- pulsul se accelerează;
- se formează umflătură.
Corpul copilului încearcă să compenseze defectul de creștere a volumului sanguin, ceea ce duce la supraîncărcare a inimii și insuficiență cardiacă severă.
Inima începe să crească în dimensiune, modificările plămânilor sunt vizibile în timpul examinării, ficatul începe să funcționeze defectuos și, de asemenea, crește. Acest defect este incompatibil cu viata si necesita o operatiune urgenta de mutare a vaselor.
Diagnosticare
Boala de inimă la un copil este adesea detectată în timpul sarcinii, apoi imediat după naștere, se efectuează o examinare pentru a confirma sau înlătura diagnosticul. La unii copii, defecte cardiace sunt detectate la programarea unui pediatru la ascultare - se aud murmurele cardiace, care nu ar trebui să fie.
Dacă se suspectează CHD, copilului i se prescrie o examinare cuprinzătoare, care poate include următoarele metode:
- Ecocardiografia fetala - ultrasonografie, care se realizează chiar și în perioada perinatală, când copilul este în pântec.
- Ecografia inimii - se efectuează pentru a detecta patologiile inimii, pentru a determina structura, dimensiunea acesteia și pentru a verifica starea vaselor de sânge și a valvelor.
- ECG - vă permite să evaluați starea mușchiului inimii.
- Monitorizarea Holter – dezvăluie aritmii ascunse și conducere cardiacă.
- Radiografia toracică - dezvăluie dimensiunea inimii și plămânilor. Uneori se efectuează cu introducerea unui agent de contrast prin cateter.
- Pulsoximetrie - verificarea nivelului de saturație de oxigen din sânge.
- RMN și CT sunt efectuate atunci când există îndoieli cu privire la diagnostic.

Diagnosticul necesită rezultatele studiilor generale și analize biochimice sânge pentru a înțelege cât de mult se schimbă compoziție chimică sânge și pentru a detecta tulburări ale organelor interne.
Cum se tratează boala cardiacă congenitală?
Tratamentul CHD depinde de severitatea patologiei, de vârsta copilului și de bolile concomitente. La majoritatea oamenilor, boala cardiacă congenitală se află în stadiul de compensare și nu amenință sănătatea de-a lungul vieții. Pentru a menține această stare, monitorizează-ți sănătatea și urmează câteva reguli:
- Supus la timp examinări cardiace.
- Refuza grele activitati fizice, limiteaza-te la sporturi usoare: gimnastica, inot sau exercitii de kinetoterapie.
- Urmează rutina zilnică, dormi suficient.
- Mănâncă sănătos, limitează aportul alimentar continut ridicat colesterolul. Controlați cantitatea de sare consumată și respectați regimul de băut.
- Evita încordare a nervilor pentru a te proteja de situații stresante.

Terapia medicamentosă are ca scop reducerea simptomelor bolii. Pentru a face acest lucru, prescrie medicamente care vizează normalizarea respirației, scăderea presiunii și eliminarea tahicardiei. Viciile de tip „alb” pot fi menținute constant terapie medicamentoasă fara interventie chirurgicala.
Anomaliile „albastre” în 90% din cazuri necesită intervenție chirurgicală în copilăria timpurie. Succesul operațiunii depinde de oportunitatea implementării acesteia. Peste 70% din operații garantează o recuperare completă a copilului. Există cazuri când operațiile pe inima unui copil au fost efectuate în uter. Dar aceste manipulări foarte complexe nu sunt folosite atât de des pe cât este necesar, deoarece majoritatea spitalelor nu au echipamentul necesarși profesioniști cu înaltă calificare.
Există o modalitate de a efectua operațiuni cu UPU:
- închis - intervenția se efectuează asupra vaselor, fără a afecta inima;
- deschis - operație abdominală efectuată pe inimă.
Când viața pacientului este amenințată, se efectuează operații de urgență. În cele mai multe cazuri, acestea sunt efectuate la o vârstă fragedă sau imediat după naștere. Intervențiile de urgență se efectuează și în condiții severe, dar este posibil să vă pregătiți pentru operație și să efectuați toate examinările necesare.
Intervențiile planificate sunt efectuate dacă nu există o amenințare directă la adresa vieții, dar operația este necesară pentru ca starea copilului să nu se agraveze. În unele cazuri, o intervenție chirurgicală este suficientă, dar, în situatii dificile poate necesita operatii repetate.
După operație, poate apărea o reapariție a defectului - stenoză vasculară, insuficiență valvulară, coarctație a aortei. Potrivit statisticilor, mai puțin de jumătate dintre copiii cu recidive trăiesc mai mult de 10 ani. În timpul protezării, există următoarele probleme- copilul crește din proteze și este nevoie de intervenții repetate, prin urmare, dacă este posibilă amânarea operației, aceasta se efectuează cât mai târziu.
Prognoza
Prognosticul bolilor cardiace congenitale la copii în majoritatea cazurilor este nefavorabil. Fără operație, bebelușii mor înainte de vârsta de doi ani din cauza insuficienței cardiace dezvoltate sau adăugării altor complicații:
- încălcarea ritmului cardiac;
- infarct miocardic;
- accident vascular cerebral;
- tromboembolism al arterelor pulmonare;
- trombocitemie;
- endocardită bacteriană;
- insuficiență respiratorie;
- reumatism al inimii;
- anevrism aortic;
- accident vascular cerebral.

Copiii cu malformații cardiace congenitale au adesea complicații ale bolilor infecțioase. sistemul respirator. Răceli aproape întotdeauna apar cu complicații care provoacă stres crescut asupra inimii. Stenoza arterei pulmonare și malformațiile combinate cresc riscul de a dezvolta tuberculoză. Din cauza circulației sanguine afectate, imunitatea copilului nu este capabilă să facă față bolii, ceea ce duce la moarte.
La copii după protezare Risc ridicat formarea de trombi la locul protezei, astfel încât trebuie să ia în mod constant diluanți ai sângelui.Cea mai mare probabilitate a unei astfel de complicații după valva tricuspidă protetică.

Copiii cu CHD sunt adesea nesiguri și instabili emoțional din cauza limitări fizice relațiile nu se dezvoltă echipa de copii. Mulți au dificultăți în învățare, ceea ce este asociat nu numai cu influența defectelor asupra sistemului nervos central, ci și cu absențe frecvente de la cursuri din cauza bolii.
Sunt furnizate unele CHD, cum ar fi defectul septului atrial sau prolapsul valvei mitrale stil de viata sanatos viata, nu randa impact negativ pe starea copilului. Cei mai mulți dintre ei învață despre defectul lor doar ca adulți.
Dacă o boală cardiacă congenitală afectează în mod semnificativ sănătatea copilului, atunci se decide chestiunea stabilirii dizabilității. În funcție de tipul și gravitatea anomaliei, se stabilește invaliditatea pe viață sau temporară. Uneori, după operație, invaliditatea este înlăturată sau se stabilește un grup mai puțin sever.